分析:书写化学方程式时,必须熟悉反应物、生成物的化学式和反应条件,必须依据质量守恒定律书写.然后根据化学方程式的特点及生成物的性质判断反应类型和反应现象.
解答:解:电解水,生成氧气和氢气,反应属于“一变多”,为分解反应.
铁丝在氧气中剧烈燃烧,火星四射,生成黑色的四氧化三铁.
木炭在高温下和氧化铜反应生成铜和二氧化碳,反应中氧化铜失去氧,作氧化剂.
二氧化碳通入水中,生成碳酸,使溶液呈酸性.
氢氧化钠溶液与硫酸铜溶液的发生复分解反应,生成硫酸钠和蓝色沉淀氢氧化铜.
故答案为:
| 化学反应 |
化学方程式 |
简 答 |
| 水的电解 |
2H2O 2H2↑+O2↑ |
反应基本类型:分解反应 |
| 铁丝燃烧 |
3Fe+2O2Fe3O4 |
实验现象:剧烈燃烧,火星四射,放热,产生黑色固体 |
| 木炭还原氧化铜 |
C+2CuO2Cu+CO2↑ |
氧化剂是:氧化铜 |
| 二氧化碳通入紫色石蕊试液 |
CO2+H2O═H2CO3 |
使紫色试液变色的物质是:碳酸 |
| 氢氧化钠溶液与硫酸铜溶液的反应 |
CuSO4+2NaOH=Na2SO4+Cu(OH)2↓ |
反应现象:有蓝色沉淀生成 |
点评:本题主要考查化学方程式的书写及化学反应中的相关知识,难度较大,要熟悉化学方程式的书写步骤和了解化学反应中的相关现象.



 新思维假期作业暑假吉林大学出版社系列答案
新思维假期作业暑假吉林大学出版社系列答案 蓝天教育暑假优化学习系列答案
蓝天教育暑假优化学习系列答案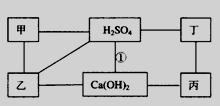 24、下图中每条连线表示两端的物质可以发生化学反应,甲、乙、丙、丁分别为Mg、BaCl2、Na2CO3、HCl中的一种.
24、下图中每条连线表示两端的物质可以发生化学反应,甲、乙、丙、丁分别为Mg、BaCl2、Na2CO3、HCl中的一种.