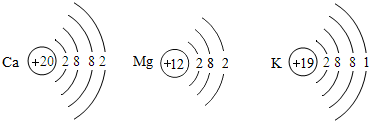
在金属活动性顺序里,位于前面的金属能把位于后面的金属从它们化合物的溶液里置换出来.
(1)CuSO4溶液中,大量存在的离子是 .
(2)将铝丝浸入CuSO4溶液中,静置,观察到的现象是 .结合现象分析,溶液中减少的离子是 ,增加的离子是 .
(3)除硫酸铜溶液外,将铝丝浸入 (任举一例)溶液中,也能产生相同的实验现象.
【答案】分析:(1)根据电离的知识,分析溶液中的离子;
(2)根据金属与盐溶液的反应,推断反应可能出现的实验现象;并分析溶液中离子的变化;
(3)由实验现象,分析置换反应所使用的盐溶液.
解答:解:(1)硫酸铜溶于水,在水的作用下硫酸铜电离成铜离子和硫酸根离子,因此溶液中大量存在铜离子和硫酸根离子;
故选Cu2+、SO42-;
(2)金属铝的活动性比铜强,铝放入硫酸铜溶液中,铝把溶液中的溶液中铜离子置换为铜附着在金属铝表面,溶液逐渐变成硫酸铝的无色溶液,金属铝变成铝离子;
故答案为:铝丝上有红色固体生成,溶液颜色变浅(或溶液由蓝色变为无色);Cu2+;Al3+;
(3)若产生相同的实验现象,则盐溶液应为铜盐,可溶性铜盐还有氯化铜、硝酸铜等;
故选CuCl2[或Cu(NO3)2].
点评:铝与硫酸铜溶液的置换反应,其实质是较活泼金属单质铝把溶液的活动性弱的金属铜的离子置换成金属单质铜的过程,反应通过电子转移实现金属间原子与离子的转换.



 阅读快车系列答案
阅读快车系列答案 学过金属的活动性顺序以后,东东对其一系列知识进行了研究.
学过金属的活动性顺序以后,东东对其一系列知识进行了研究.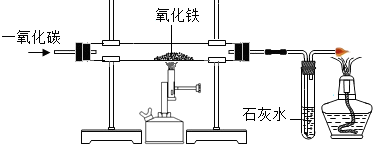 铁、铝、铜是日常生活中使用最广泛的金属.
铁、铝、铜是日常生活中使用最广泛的金属.