
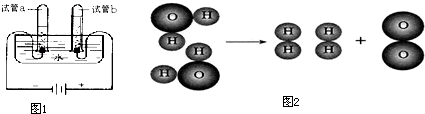
 (1)如图1所示的是电解水实验装置.通电一段时间后,在两个试管中分别收集到气体a和气体b. 请回答:
(1)如图1所示的是电解水实验装置.通电一段时间后,在两个试管中分别收集到气体a和气体b. 请回答:| 通电 |
| 通电 |
| 1 |
| 4 |
| 验证 | 方 法 | 现 象 |
| 鳔内含O2 | 将燃着的木条放入含有鱼鳔内气体的集气瓶中 将燃着的木条放入含有鱼鳔内气体的集气瓶中 |
木条燃烧情况变化不大 木条燃烧情况变化不大 |
| 鳔内含CO2 | 在含有鱼鳔内气体的集气瓶中加入少量的澄清石灰水 在含有鱼鳔内气体的集气瓶中加入少量的澄清石灰水 |
石灰水变浑浊 石灰水变浑浊 |
| 通电 |
| 通电 |
| 实验目的 | 方法 | 现象 |
| 将燃着的木条放入含有鱼鳔内气体的集气瓶中 | 木条燃烧情况变化不大 | |
| 在含有鱼鳔内气体的集气瓶中加入少量的澄清石灰水 | 石灰水变浑浊 |


科目:初中化学 来源: 题型:阅读理解
| 通电 |
| 通电 |
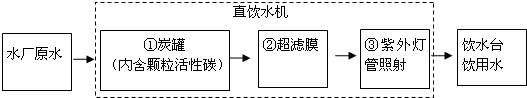
查看答案和解析>>
科目:初中化学 来源: 题型:阅读理解
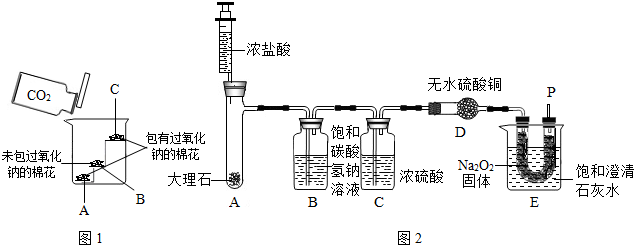
查看答案和解析>>
科目:初中化学 来源: 题型:
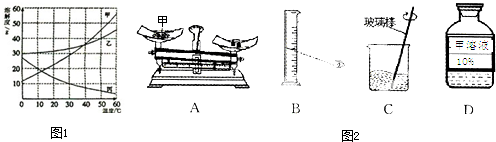
查看答案和解析>>
科目:初中化学 来源: 题型:

| 反应前后质量组别 | 甲组 | 乙组 | 丙组 |
| 盐酸与碳酸钠粉末反应前称量(g) | 85.3 | 82.8 | 86.5 |
| 盐酸与碳酸钠粉末反应后称量(g) | 85.3 | 80.6 | 87.8 |
查看答案和解析>>
科目:初中化学 来源:2012年江苏省无锡市滨湖中学中考化学二模试卷(解析版) 题型:解答题

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com