
| A. | X的化学式是C5H12O6 | B. | X中碳、氢两种元素的质量比为1:2 | ||
| C. | X的相对分子质量是174 | D. | X中碳元素的质量分数为40% |
分析 由题意,知反应的化学方程式为X+6O2$\frac{\underline{\;一定条件\;}}{\;}$6CO2+6H2O,根据质量守恒定律的有关知识,化学反应前后元素的种类不变,原子个数不变,元素质量不变,可推测X的化学式,然后依次分析各选项.
解答 解:由题意,知反应的化学方程式为X+6O2$\frac{\underline{\;一定条件\;}}{\;}$6CO2+6H2O,根据质量守恒定律的意义,则X的一个分子中含有6个碳原子、12个氢原子、6个氧原子,则X的化学式为C6H12O6,则:
A、X的化学式是C6H12O6,故说法错误;
B、X中碳、氢两种元素的质量比为(12×6):(1×12)=6:1,故说法错误;
C、X的相对分子质量是12×6+1×12+16×6=180,故说法错误;
D、X中碳元素的质量分数为:$\frac{12×6}{180}$×100%=40%,故说法正确.
故选D.
点评 掌握有关化学式的计算和推断方法;掌握质量守恒定律的内容及其应用;掌握相对分子质量的计算、元素质量比的计算、元素质量分数的计算的方法,此题难度不大.


 名校课堂系列答案
名校课堂系列答案科目:初中化学 来源: 题型:选择题
| A. | 通过煮沸方法使硬水软化 | |
| B. | NaCl和NaNO2(亚硝酸钠)都有咸味,都可用作食物的调味品 | |
| C. | 在发酵的面团中加入小苏打以提高馒头的口感和除去酸味 | |
| D. | 加热,观察外形变化鉴别热塑性塑料和热固性塑料 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
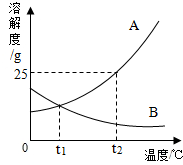 如图是A、B两种固体物质的溶解度曲线,下列说法错误的是( )
如图是A、B两种固体物质的溶解度曲线,下列说法错误的是( )| A. | A物质中混有少量的B物质,可用降温结晶的方法提纯A | |
| B. | t1℃时,A物质和B物质的饱和溶液中溶质的质量分数一定相等 | |
| C. | 将t2℃时,A和B的饱和溶液降温到t1℃,所得溶液中溶质的质量分数相等 | |
| D. | t2℃时,将20gA物质加入50g水中,所得溶液中溶质的质量分数为20% |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 60% | B. | 70% | C. | 80% | D. | 无法确定 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题

查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com