
为了测定某石灰石中碳酸钙的质量分数,准确称取12.5g石灰石样品,研碎后放入烧杯中,向其中加入足量稀盐酸,(杂质不与盐酸反应,也不溶于水),实验测得的数据如下图所示。(注:CaCO3+2HCl=CaCl2+H2O+CO2↑)
(1)将石灰石样品研碎的目的是 。
(2)12.5g样品完全反应生成二氧化碳的质量m= g。
(3)求该石灰石样品中碳酸钙的质量分数。
(1)增大石灰石与稀盐酸的接触面积(或加快反应速率,使反应更为充分)
(2)4.4g。
(3)解:12.5g样品中碳酸钙的质量为X
CaCO3+2HCl=CaCl2+H2O+CO2↑
100 44
X 4.4g
100/44=X/4.4g
X=10g
样品中CaCO3%=10g÷12.5g×100% = 80%
答:该石灰石样品中碳酸钙的质量分数为80%。
解析试题分析:解:(1)将石灰石样品研碎的目的是增大石灰石与稀盐酸的接触面积,加快反应速率,使反应更为充分。
(2)由图示可得,50g稀盐酸反应之后产生二氧化碳2.2g,则100g稀盐酸反应完全后,反应中好结束,产生的二氧化碳为4.4g,故12.5g样品完全反应生成二氧化碳的质量m=4.4g。
(3)解:12.5g样品中碳酸钙的质量为X
CaCO3+2HCl=CaCl2+H2O+CO2↑
100 44
X 4.4g
100/44=X/4.4g
X=10g
样品中CaCO3%=10g÷12.5g×100% = 80%
答:该石灰石样品中碳酸钙的质量分数为80%。
考点:根据化学方程式计算。
点评:根据化学方程式计算,要注意解题的步骤,设、写、找、列、解、答。


 新思维假期作业暑假吉林大学出版社系列答案
新思维假期作业暑假吉林大学出版社系列答案 蓝天教育暑假优化学习系列答案
蓝天教育暑假优化学习系列答案科目:初中化学 来源: 题型:阅读理解
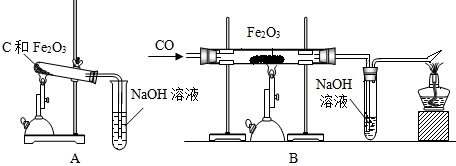
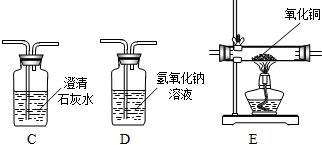
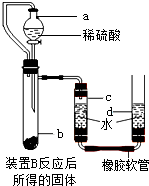
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
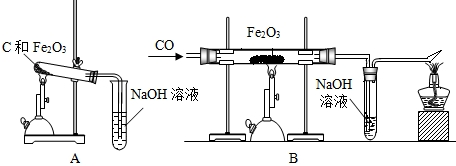
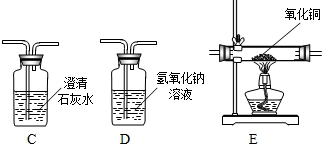
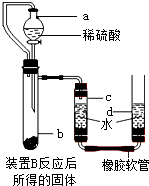
查看答案和解析>>
科目:初中化学 来源:专项题 题型:实验题



查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com