
| A. | 用带火星的木条鉴别空气和氧气 | B. | 用澄清石灰水鉴别CO2和CO | ||
| C. | 用闻气味法鉴别酒精和白醋 | D. | 用点燃法鉴别棉纤维和羊毛 |
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
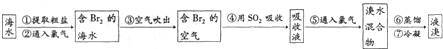
| 温度 溶解度/g 盐 | 10℃ | 20℃ | 30℃ | 40℃ | 50℃ |
| 氯化钠 | 35.8 | 36.0 | 36.3 | 36.6 | 37.0 |
| 碳酸氢铵 | 15.8 | 21.0 | 27.0 | ||
| 碳酸氢钠 | 8.1 | 9.6 | 11.1 | 12.7 | |
| 氯化铵 | 33.3 | 37.2 | 41.4 | 45.8 | 50.4 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
 某品牌天然矿泉水标签的部分内容如图所示,请用正确的化学用语完成下列问题:
某品牌天然矿泉水标签的部分内容如图所示,请用正确的化学用语完成下列问题:查看答案和解析>>
科目:初中化学 来源: 题型:解答题
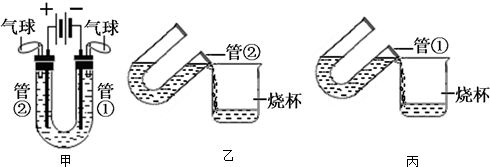
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
| 菜肴 | 半小时 | 6小时 | 18小时 | 24小时 |
| 炒青菜 | 0.6861 | 0.7982 | 4.3333 | 5.3624 |
| 韭菜炒蛋 | 1.8153 | 1.9249 | 2.8390 | 5.6306 |
| 红烧肉 | 2.4956 | 4.2558 | 4.3668 | 5.5188 |
| 红烧鲫鱼 | / | 2.0948 | 3.2300 | 7.2397 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com