
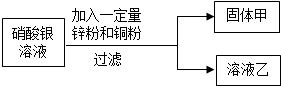
分析 根据三种金属的活动性由强到弱的顺序:锌>铜>银,把一包铜粉和锌粉的混合物放入一定量的硝酸银溶液中,使其充分反应后过滤,判断铜、锌混合物与硝酸银充分反应的结果分析滤渣和滤液的成分;依据实验现象“得到蓝色溶液”,判断铜、锌混合物与硝酸银充分反应的结果分析滤渣和滤液的成分等.
解答 解:(1)由得到乙溶液呈蓝色,说明铜粉与硝酸银发生了反应,反应后溶液中一定含有硝酸铜;由于锌的活动性比铜强,锌会先于铜与硝酸银反应且锌粉可与硝酸铜反应,因此可判断锌粉已完全反应,溶液中一定含有硝酸锌;硝酸银是否完全反应则成为所要猜测的两种可能,若硝酸银完全反应,则溶液中只含有硝酸锌、硝酸铜,若硝酸银有剩余,则溶液中含有硝酸锌、硝酸铜、硝酸银;因此滤渣中一定含有银,一定没有锌,可能含有铜;故向固体甲上滴加盐酸时没有气泡产生;
(2)若溶液乙为无色溶液,则固体甲的成分中一定有的物质是铜、银或Cu、Ag,可能有的物质是锌或Zn.
(3)若溶液乙为无色溶液,则固体甲的成分中一定有的物质是铜、银或Cu、Ag,则向固体中滴加硝酸银溶液,则化学方程式为:Cu+2AgNO3=Cu(NO3)2+2Ag.
故答案为:
(1)没有.(2)铜、银,锌.(3)Cu+2AgNO3=Cu(NO3)2+2Ag.
点评 本题考查了金属的活动性顺序的运用,活动性强的金属放入活动性弱的金属的混合盐溶液中,活动性强的金属会先把活动性最弱的金属从其盐溶液中置换出来,然后再置换活动性较弱的金属.


 53随堂测系列答案
53随堂测系列答案科目:初中化学 来源: 题型:填空题
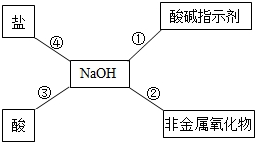 归纳总结是学习科学的重要方法之一,晓明同学用图总结了NaOH的四条化学性质(即NaOH与四类物质能够发生化学反应).
归纳总结是学习科学的重要方法之一,晓明同学用图总结了NaOH的四条化学性质(即NaOH与四类物质能够发生化学反应).查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | Ba2+:一个钡离子带2个单位正电荷 | |
| B. | CO2:二氧化碳中含有2个氧元素 | |
| C. | 2H:2个氢原子 | |
| D. | $\stackrel{+2}{Ca}$O:氧化钙中钙元素的化合价为+2价 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 只有氢氧才是碱不可缺少的元素 | B. | 有涩味的物质 | ||
| C. | 一切碱中都含有金属元素 | D. | 与酸作用时失去原有性质的物质 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 分子可以构成物质,而原子只能构成分子 | |
| B. | 原子的质量几乎都集中在原子核中 | |
| C. | 在化学变化中,分子可以分成原子,而原子不能再分 | |
| D. | 当原子失去或者得到电子后,其性质发生了改变 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
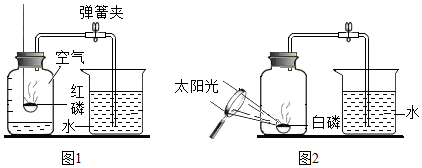 (1)如图1是测定空气中氧气体积分数的实验示意图.①实验时,取下橡皮塞,点燃红磷迅速伸入集气瓶中并塞紧橡皮塞,待反应结束装置冷却至室温后,打开弹簧夹,能观察到的现象是烧杯中的水将流入集气瓶内约到刻度1处.
(1)如图1是测定空气中氧气体积分数的实验示意图.①实验时,取下橡皮塞,点燃红磷迅速伸入集气瓶中并塞紧橡皮塞,待反应结束装置冷却至室温后,打开弹簧夹,能观察到的现象是烧杯中的水将流入集气瓶内约到刻度1处.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com