
| 氢氧化钠 | 氯化钠 | 氢氧化钙 | 碳酸钠 | |
| 溶解度/g(20℃) | 51 | 36 | 0.16 | 21.5 |
| 实验步骤 | 实验现象 | 实验结论 |
| 取少量样品溶液于试管中,滴加________. | ________ | 该溶液是碳酸钠溶液. 有关反应的化学方程式为: ________. |
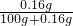 ×100%<0.16%,而该溶液溶质质量分数为10%,故不可能是氢氧化钙溶液;
×100%<0.16%,而该溶液溶质质量分数为10%,故不可能是氢氧化钙溶液;

 阅读快车系列答案
阅读快车系列答案科目:初中化学 来源: 题型:
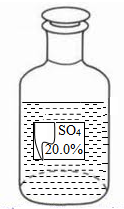 小华同学在化学实验室发现一瓶盛有无色溶液的试剂瓶,其标签严重破损(如右图所示).老师告诉他,这瓶试剂可能是硫酸、硫酸钠、硫酸镁溶液中的一种.小华同学通过查阅资料得知,常温下这三种物质的溶解度如下表:
小华同学在化学实验室发现一瓶盛有无色溶液的试剂瓶,其标签严重破损(如右图所示).老师告诉他,这瓶试剂可能是硫酸、硫酸钠、硫酸镁溶液中的一种.小华同学通过查阅资料得知,常温下这三种物质的溶解度如下表:| 物质 | H2SO4 | Na2SO4 | MgSO4 |
| 溶解度/g | 与水任意比互溶 | 19.0 | 39.0 |
| 实验步骤 | 实验现象 | 实验结论 |
查看答案和解析>>
科目:初中化学 来源: 题型:
| 实验步骤 | 实验现象 | 实验结论 |
| 取少量溶液于试管中,滴加 氯化钙溶液(或稀盐酸) 氯化钙溶液(或稀盐酸) |
产生白色沉淀(或有气泡冒出) 产生白色沉淀(或有气泡冒出) |
该溶液是碳酸钠溶液 |
查看答案和解析>>
科目:初中化学 来源: 题型:阅读理解
| 氢氧化钠 | 氯化钠 | 氢氧化钙 | 碳酸钠 | |
| 溶解度/g(20℃) | 51 | 36 | 0.16 | 21.5 |
| 实验步骤 | 实验现象 | 实验结论 |
| 取少量样品溶液于试管中,滴加 稀盐酸 稀盐酸 . |
有气泡产生 有气泡产生 |
该溶液是碳酸钠溶液. 有关反应的化学方程式为: Na2CO3+2HCl═2NaCl+H2O+CO2↑ Na2CO3+2HCl═2NaCl+H2O+CO2↑ . |
查看答案和解析>>
科目:初中化学 来源:2011-2012学年江苏省宿迁市沭阳县广宇学校九年级(下)第二次月考化学试卷(解析版) 题型:解答题
| 氢氧化钠 | 氯化钠 | 氢氧化钙 | 碳酸钠 | |
| 溶解度/g(20℃) | 51 | 36 | 0.16 | 21.5 |
| 实验步骤 | 实验现象 | 实验结论 |
| 取少量样品溶液于试管中,滴加______. | ______ | 该溶液是碳酸钠溶液. 有关反应的化学方程式为: ______. |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com