
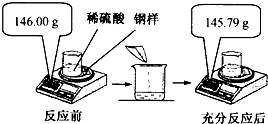
 钢的含碳量为0.03%~2%.为测定某钢样的含碳量是否合格,取该钢样粉末6.00g(假设钢样中仅含Fe和C)和足量稀硫酸按如图所示操作.根据所得数据计算:
钢的含碳量为0.03%~2%.为测定某钢样的含碳量是否合格,取该钢样粉末6.00g(假设钢样中仅含Fe和C)和足量稀硫酸按如图所示操作.根据所得数据计算: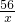 =
=
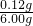 ×100%=2%
×100%=2%

 阅读快车系列答案
阅读快车系列答案科目:初中化学 来源: 题型:
查看答案和解析>>
科目:初中化学 来源: 题型:
查看答案和解析>>
科目:初中化学 来源: 题型:
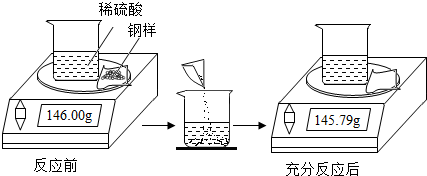 (2013?葫芦岛)钢的含碳量为0.03%~2%.为测定某钢样的含碳量是否合格,取该钢样粉末6.00g(假设钢样中仅含Fe和C)和足量稀硫酸按如图所示操作.根据所得数据计算:
(2013?葫芦岛)钢的含碳量为0.03%~2%.为测定某钢样的含碳量是否合格,取该钢样粉末6.00g(假设钢样中仅含Fe和C)和足量稀硫酸按如图所示操作.根据所得数据计算:查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com