
日常使用的金属材料,大多数属于合金。黄铜是以锌作主要添加元素的铜合金。
⑴赤铜(Cu2O)是我国古代制取黄铜的一种原料。Cu2O中铜元素与氧元素的质量比是  。
。
⑵弹壳的黄铜只含有锌和铜。将22 g弹壳放在盛有100 g稀硫酸的烧杯中(硫酸足量),当弹壳不再溶解后,烧杯中混合物的质量是121. 8 g。计算:
①产生氢气的质量。
②弹壳中铜的质量。
③反应后所得溶液中ZnSO4的质量分数(计算结果保留一位小数)。
【答案】⑴64×2:16=8:1
⑵①22g+100g-121.8g=0.2g
②设参加反应的Zn的质量为x,设反应生成ZnSO4的质量为y
Zn + H2SO4 = ZnSO4 + H2↑
65 161 2
22g-x y 0.2g
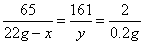
x=15.5g y =16.1g
反应后所得溶液中ZnSO4的质量分数= 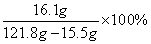 =15.1%
=15.1%
答:产生氢气的质量为0.2g;弹壳中的铜质量为15.5g;反应后所得溶液中ZnSO4的质量分数为15.1%。
【解析】⑴ Cu2O铜元素与氧元素的质量比 64×2:16=8:1
⑵①产生氢气的质量为加入物质的总质量与反应后剩余物质的总质量之差22g+100g-121.8g=0.2g
②由H2的质量可以求出参加反应的Zn和反应生成的ZnSO4。原弹壳为22 g只含有锌和铜,从而求出铜;反应后所得溶液为烧杯中混合物的质量减去未参加反应的物质(铜)。


 阅读快车系列答案
阅读快车系列答案科目:初中化学 来源: 题型:
有三瓶无色无味的气体,分别是氧气、空气、二氧化碳,区别它们最简单的方法是( )
A.伸入燃烧的木条 B. 测定气体的密度
C.滴入澄清石灰水,振荡 D. 滴入紫色石蕊试液,振荡
查看答案和解析>>
科目:初中化学 来源: 题型:
将镁粉和铝粉的混合物7.2g与足量的氧气充分反应,得到的氧化物质量可能为( )
A. 10.6g B. 12.0g C. 13.0g D.13.6g
查看答案和解析>>
科目:初中化学 来源: 题型:
将4.0g Cu—Zn合金粉末放到盛有10g稀硫酸的烧杯中,恰好完全反应。过滤,称量滤液的质量,相关实验数据如下:
| 反应前物质质量/g | 反应后物质质量/g | |
| Cu—Zn合金 | 稀硫酸 | 滤液质量 |
| 4.0 | 10 | 11.26 |
⑴Cu—Zn合金属于 材料(填“金属”或“有机合成”)。
⑵若不考虑该合金中除Cu、Zn以外的其它成分,请计算原Cu—Zn合金中Zn的质量。写出必要的计算过程。(Zn-65 Cu-63.5 H-1 O-16 S-32)
查看答案和解析>>
科目:初中化学 来源: 题型:
实验中学化学兴趣小组为测定某石灰石样品(杂质不溶于水,也不与酸反应)中碳酸钙的质量分数,进行如图所示的实验。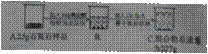
请根据以上信息计算:
(1)样品中碳酸钙的质量分数?
(2)C烧杯中溶液的溶质质量分数?
查看答案和解析>>
科目:初中化学 来源: 题型:
为测定某CuSO4溶液的溶质质量分数。化学小组的同学取CuSO4溶液100g,向其中滴加一定浓度的NaOH溶液,至不再产生沉淀为止,共用去NaOH溶液80g,过滤,得到滤液175.1g。请计算:
(1)该反应生成沉淀_____g;
(2)该硫酸铜溶液的溶质质量分数。
(温馨提示:CuSO4+2NaOH=Cu(OH)2↓+Na2SO4)
查看答案和解析>>
科目:初中化学 来源: 题型:
向某铁粉样品中,加入溶质质量分数为20﹪的硫酸铜溶液80g,恰好完全反应(样品中杂质不溶于水也不与硫酸铜反应)。请结合下图提供的数据计算:
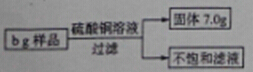
(1)b的数值。
(2)向不饱和溶液中加入120.8g水,求所得溶液中溶质的质量分数。
查看答案和解析>>
科目:初中化学 来源: 题型:
某氢氧化钙中含碳酸钙杂质。称取研细的该样品12.4g放入锥形瓶中,加入32.6g的水,充分振荡形成悬浊液,再向锥形瓶中逐滴滴加盐酸使其充分反应至无气泡产生。测得加入盐酸的质量与锥形瓶中的物质的质量关系如下表示。
| 加入盐酸的质量g | 0 | 25 | 37.5 |
| 锥形瓶中物质的质量 | 45 | 70 | 80.3 |
(1)加入盐酸的质量在0—25g时, 与盐酸发生反应。
(2)反应产生二氧化碳质量为 g。
(3)求样品中氢氧化钙的质量分数(写出计算过程,精确到0.1%)。
查看答案和解析>>
科目:初中化学 来源: 题型:
现有20g含Fe2O3为80%的赤铁矿石,加入到150g稀盐酸中,恰好完全反应(铁矿石中杂质都不溶于水,且不与稀盐酸反应)。(计算结果保留一位小数)
求:(1)赤铁矿石中的质量为 g,其中铁元素的质量为 g。
(2)稀盐酸中溶质的质量分数;
(3)恰好完全反应后所得溶液中溶质质量分数。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com