
| 物质 | 20℃时溶解度/g | 相对分子质量 |
| Na2CO3 | 21.5 | 106 |
| NaHCO3 | 9.6 | 84 |
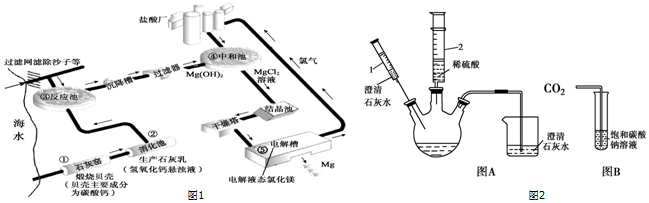
分析 (1)①中碳酸钙在高温条件下分解生成氧化钙和二氧化碳,②中氧化钙和水反应生成氢氧化钙,③中氢氧化钙和氯化镁反应生成氢氧化镁沉淀和氯化钙,④中氢氧化镁和稀盐酸反应生成氯化镁和水,⑤中电解氯化镁生成镁和氯气;
(2)碳酸钠溶液显碱性,能使酚酞试液变红色;
碳酸钠和氢氧化钙反应生成碳酸钙沉淀和氢氧化钠,和稀盐酸反应生成氯化钠、水和二氧化碳;
碳酸钠和水、二氧化碳反应生成碳酸氢钠.
解答 解:(1)①中碳酸钙在高温条件下分解生成氧化钙和二氧化碳,属于分解反应,②中氧化钙和水反应生成氢氧化钙,属于化合反应,③中氢氧化钙和氯化镁反应生成氢氧化镁沉淀和氯化钙,属于复分解反应,④中氢氧化镁和稀盐酸反应生成氯化镁和水,属于复分解反应,⑤中电解氯化镁生成镁和氯气,属于分解反应,因此在①~⑤中发生分解反应的装置有①⑤;
I装置③内,氢氧化钙和氯化镁反应生成氢氧化镁沉淀和氯化钙,发生反应的化学方程式为:MgCl2+Ca(OH)2═Mg(OH)2↓+CaCl2.
故填:①⑤;MgCl2+Ca(OH)2═Mg(OH)2↓+CaCl2.
(2)①步骤二:将注射器1的针头向瓶内推进,使针头下端进入瓶内液面下,向外拉注射器,此时注射器1中,碳酸钠和氢氧化钙反应生成碳酸钙沉淀和氢氧化钠,反应的化学方程式为:Na2CO3+Ca(OH)2═CaCO3↓+2NaOH.
故填:Na2CO3+Ca(OH)2═CaCO3↓+2NaOH.
步骤三:将注射器2的足量稀盐酸全部推进瓶内,稀盐酸和碳酸钠反应生成氯化钠、水和二氧化碳,溶液由碱性变成中性,能观察到溶液由红色变成无色,产生气泡.
故填:溶液由红色变成无色,产生气泡.
步骤四:则此溶液中一定含有的溶质(除酚酞外)为反应生成的氯化钠和氯化钙.
故填:氯化钠、氯化钙.
②将二氧化碳持续通入饱和碳酸钠溶液中时,碳酸钠和水、二氧化碳反应生成碳酸氢钠,反应的化学方程式为:Na2CO3+H2O+CO2=2NaHCO3.
故填:Na2CO3+H2O+CO2=2NaHCO3.
点评 本题主要考查物质的性质,解答时要根据各种物质的性质,结合各方面条件进行分析、判断,从而得出正确的结论.


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案 目标测试系列答案
目标测试系列答案科目:初中化学 来源: 题型:选择题
| A. | Na2SO4、Ba(OH)2、H2SO4 | B. | Na2CO3、AgNO3、HCl | ||
| C. | AgNO3、CaCl2、HNO3 | D. | NaOH、MgCl2、H2SO4 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | ①④ | B. | ①② | C. | ②④ | D. | ①②④ |
查看答案和解析>>
科目:初中化学 来源: 题型:计算题
| 加入稀盐酸的次序 | 1 | 2 | 3 | 4 |
| 加入稀盐酸的质量(克) | 10 | 10 | 10 | 10 |
| 剩余固体的质量(克) | 4.0 | m | 1.2 | 1.2 |
查看答案和解析>>
科目:初中化学 来源: 题型:推断题
查看答案和解析>>
科目:初中化学 来源: 题型:推断题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
 如图,在盛有一定质量分数稀硫酸的容器中,放一塑料方块.刚好能悬浮于稀硫酸中,若向容器中加入少量氯化钡溶液后,则塑料方块在溶液中( )
如图,在盛有一定质量分数稀硫酸的容器中,放一塑料方块.刚好能悬浮于稀硫酸中,若向容器中加入少量氯化钡溶液后,则塑料方块在溶液中( )| A. | 下沉 | B. | 上浮 | C. | 不变 | D. | 无法判断 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com