考点:电解水实验,实验室制取氧气的反应原理,催化剂的特点与催化作用,质量守恒定律及其应用
专题:元素化合物知识型
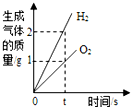
分析:A、根据电解水时产生的氢气和氧气的体积比是2:1,质量比为1:8,进行分析判断;
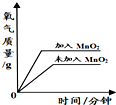
B、根据用等质量、等浓度的双氧水分别制取氧气,有无催化剂只是改变化学反应的速率,不影响生成氧气的量进行解答;
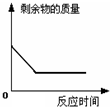
C、根据高锰酸钾受热分解生成锰酸钾、二氧化锰和氧气进行解答;
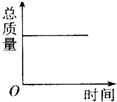
D、根据质量守恒定律进行解答.
解答:解:A、将水通电电解一段时间,水通电产生氢气和氧气的体积比是2:1,质量比为1:8,所以图象不能正确反映对应变化关系,故A错误;
B、用等质量、等浓度的双氧水分别制取氧气,有无催化剂只是改变化学反应的速率,不影响生成氧气的量,所以最终生成氧气的质量应该相等,故B错误;
C、高锰酸钾受热分解生成锰酸钾、二氧化锰和氧气,生成的氧气逸出,所以剩余物质的质量会减少,当反应完毕后质量不再改变,所以图象能正确反映对应变化关系,故C正确;
D、根据质量守恒定律可知,木炭在耐高温的密闭容器中(含空气)加热,反应前后质量,所以图象能正确反映对应变化关系,故D正确.
故选:CD.
点评:本题是一道图象坐标与化学知识相结合的综合题,解题的关键是结合所涉及的化学知识,正确分析各变化的过程,注意分析坐标轴表示的意义、曲线的起点、折点及变化趋势,进而确定正确的图象.



 能力评价系列答案
能力评价系列答案 唐印文化课时测评系列答案
唐印文化课时测评系列答案 导学与测试系列答案
导学与测试系列答案