
下列四个图象分别与选项中的操作相对应,其中合理的是( )
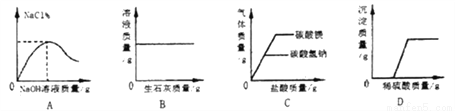
A. 向一定质量的盐酸中滴加氢氧化钠溶液
B. 向一定质量的饱和石灰水中加入生石灰
C. 等质量的碳酸镁和碳酸氢钠中加入足量的稀盐酸
D. 向一定量的氢氧化钠和硝酸钡的混合溶液中滴加稀硫酸
A 【解析】A. 向一定量盐酸中滴加氢氧化钠溶液。故A正确。 B. 向一定量的饱和石灰水中加入生石灰,生石灰与水反应,生成氢氧化钙,溶液质量减少。故B错误。C. 向等质量的碳酸镁和碳酸氢钠中分别加入足量稀盐酸,根据化学方程式知,生成二氧化碳质量相等。故C错误。D. 向一定量的氢氧化钠和硝酸钡的混合溶液中滴加稀硫酸,同时与氢氧化钠反应,硝酸钡反应。故D错误。 点睛∶本题主要考查用图像表示...科目:初中化学 来源:湖北省宣恩县2018届九年级第二次质量检测化学试卷 题型:简答题
在宏观、微观和符合之间建立联系是化学学科的特点。
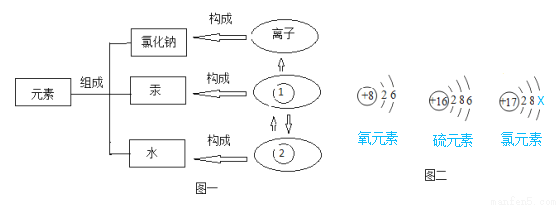
(1)物质的组成及构成关系如图1所示,图中①表示的是_________,②表示的是_________。
(2)下列说法正确的是______(填字母)。
A.氯化氢是由氢、氯两种元素组成的
B.氯化氢是由氢气和氯气混合而成的
C.氯化氢是是由一个氢原子和一个氯原子构成的
(3)如图二所示是氧、硫、氯三种元素的原子结构示意图。
①氯原子结构示意图中X的数值是_________,
②氧和硫两种元素的化学性质具有相似性的原因是它们的原子的___________________相同。
原子 分子 A 7 最外层电子数 【解析】本题考查了物质的宏观组成和微观构成的知识,完成此题,可以依据已有的知识进行。了解原子结构示意图的意义是正确解题的关键。 (1)汞是金属,是由原子构成的,水是由水分子构成; (2)A、氯化氢是由氢、氯两种元素组成的,正确;B、氯化氢属于纯净物,是由氢、氯两种元素组成的,错误;C、氯化氢是由氯化氢分子构成,一个氯化氢分子是由一个氢原子和一个氯...查看答案和解析>>
科目:初中化学 来源:江苏省镇江市润州区2018届九年级第二次模拟考试化学试卷 题型:多选题
NH4Cl和Na2SO4的溶解度表及溶解度曲线如下。下列说法正确的是
温度/℃ | 10 | 20 | 30 | 40 | 50 | 60 | |
溶解度 S/g | NH4Cl | 33.3 | 37.2 | 41.4 | 45.8 | 50.4 | 60.2 |
Na2SO4 | 9.6 | 20.2 | 40.8 | 48.4 | 47.5 | 47.0 |
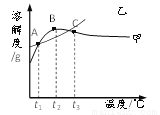
A. 甲为NH4Cl
B. t3℃应介于40℃~50℃
C. 乙物质的饱和溶液从t2升温到t3,溶液的溶质质量分数不变
D. 甲、乙饱和溶液从t3降温到t1,析出晶体(均不带结晶水)的质量一定相等
BC 【解析】根据所学知识和题中信息知,A、甲为硫酸钠,乙为NH4Cl,故A错误;B、t3℃应介于40℃~50℃,故B正确;C、乙物质的饱和溶液从t2升温到t3,溶解度随温度升高而增大,溶液的溶质质量分数不变,故C正确;D、甲、乙饱和溶液从t3降温到t1,由于溶液没有量的限制,析出晶体(均不带结晶水)的质量不一定相等,故D错误。 点睛∶溶解度曲线的意义①表示同一种物质在不同温度时的溶解...查看答案和解析>>
科目:初中化学 来源:河南省信阳市2018届九年级下学期最后一次模拟考试化学试卷 题型:综合题
化学实验是进行科学探究的重要方式。

(1)写出一个用A装置制取气体的化学方程式____________________
(2)实验室可用氯化钠固体和浓硫酸在加热条件下反应制取氯化氢气体,该气体极易溶于水,有刺激性气味。若要制取并收集一瓶干燥的氯化氢,并有效防止散失大气中,请选择所需要的装置,装置中导管口连接的顺序为__________。制取氯化氢的化学方程式为_________。
(3)趣味实验:如图,实验时,在水中滴入紫色石蕊溶液,将胶头滴管中水挤入盛有干燥氯化氢气体的烧瓶中,打开橡皮管上的止水夹,可观察到什么现象________?为什么__________?
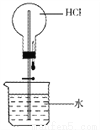
(4)干燥的碳酸钠粉末放入氯化氢的气体中,不反应。但放入盐酸中却能反应。请从微观角度解释不反应的原因________。对于盐酸而言,溶质的质量分数越大,溶液的酸性越强。常温下,10%的稀盐酸的pH____(填“大于”、“小于”或“等于”)12%的稀盐酸的pH。
(5)取12.5 g石灰石于烧杯中,向其中加入100 g足量的稀盐酸,充分反应后(杂质不参加反应),烧杯中固液混合物的质量为108.1 g,请计算该石灰石中碳酸钙的质量分数___________。
2KMnO4 K2MnO4 + MnO2 + O2↑ c-i-h-d-e-g 2 NaCl + H2SO4 Na2SO4 + 2 HCl↑ 烧杯中的水进入烧瓶,形成红色喷泉; 氯化氢溶于水使烧瓶内压强减小,烧杯中的水进入烧瓶,形成喷泉,石蕊遇酸性溶液变红色。 氯化氢是分子构成的,没有H+ 所以与碳酸钠粉末不反应; 大于 80% 【解析】(1)A装置试管口有棉团,适用于高锰酸钾制氧气,化学方程...查看答案和解析>>
科目:初中化学 来源:河南省信阳市2018届九年级下学期最后一次模拟考试化学试卷 题型:填空题
若粗盐中含有Na2SO4、MgCl2、CaCl2三种杂质,加入正确的除杂试剂后,得到的沉淀中盐的化学式为________ ,过滤后滤液中溶质有 _____种,若加入过量稀盐酸,则造成所得精盐的质量_______(填偏大、偏小、不变)。
BaCO3 CaCO3 BaSO4 三 不变 【解析】若粗盐中含有Na2SO4、MgCl2、CaCl2三种杂质,除去钙离子选用碳酸钠、除去镁离子使用氢氧化钠、除去磷酸根离子选用氯化钡,由于含有多种杂质,所以加入的除杂试剂要考虑加入试剂的顺序,加入过量氯化钡溶液的顺序应该在加入碳酸钠溶液之前,以保证将过量的氯化钡除去,过滤后,最后加入盐酸,除去过量的碳酸钠,而氢氧化钠溶液只要在过滤之前加入就可...查看答案和解析>>
科目:初中化学 来源:河南省信阳市2018届九年级下学期最后一次模拟考试化学试卷 题型:单选题
下列各组物质充分反应后,溶液质量比反应前的溶液质量减小的是 ( )
A. 铁片浸入稀硫酸中 B. 锌片浸入硫酸铜溶液中
C. 氯化铵溶液加入烧碱溶液中 D. 碳酸氢钠粉末加入稀盐酸中.
C 【解析】A、铁与稀硫酸反应,生成氢气,逸出气体的质量<参加反应铁的质量,故溶液质量比反应前的溶液质量增加,错误;B、锌与硫酸铜反应,生成硫酸锌和铜,因为锌的相对原子质量>铜的相对原子质量,故置换出的铜的质量<参与反应锌的质量,故溶液质量增加,错误;C、氯化铵溶液加入烧碱溶液中发生反应生成氨气逸出,所以溶液质量比反应前的溶液质量减小,正确;D、碳酸氢钠粉末加入稀盐酸中生成氯化钠、水和二氧化...查看答案和解析>>
科目:初中化学 来源:河南省信阳市2018届九年级下学期最后一次模拟考试化学试卷 题型:单选题
下列过程中不涉及化学变化的是( )
A. 铁矿石冶炼成铁 B. 石灰石等物质烧制玻璃
C. 葡萄酿成红酒 D. 直饮水机中活性炭吸附杂质
D 【解析】A、铁矿石冶炼成铁的过程中有新物质铁等生成,属于化学变化,错误;B、石灰石等物质烧制玻璃的过程中,有新物质生成,属于化学变化,错误;C、葡萄酿成红酒的过程中,有新物质酒精等生成,属于化学变化,错误;D、直饮水机中活性炭吸附杂质的过程中,只是吸附异味和色素,没有新物质生成,属于物理变化,正确。故选D。查看答案和解析>>
科目:初中化学 来源:山东省泰安市2018年中考化学试卷 题型:计算题
儿童缺锌会引起食欲不振、发育不良等症状。如图为某补锌口服液说明书的部分信息,图中葡萄糖酸锌化学式已不完整,请根据相关信息回答下列问题:

(1)葡萄糖酸锌的化学式量是455,则葡萄糖酸锌化学式氢原子右下角的数字为__;
(2)若儿童lkg体重每日需要0.5mg锌,每天从食物中只能摄入所需锌的一半。体重为20kg的儿童,理论上一天还需服该口服液__支?
221 【解析】 本题考查了根据化学式进行计算,结合新信息,灵活运用化学式的意义和标签上信息是解题的关键。 (1)设:葡萄糖酸锌化学式中氢原子右下角的数字为x,根据葡萄糖酸锌化学式,葡萄糖酸锌的相对分子质量:12×12+x+16×14+65=455,x=22; (2)儿童1kg体重每日需要0.5mg锌,体重为20kg的儿童每日需要锌=0.5mg×=10mg;其中一半由口服液...查看答案和解析>>
科目:初中化学 来源:湖北省利川市2018届九年级第一次质量检测化学试卷 题型:计算题
恩施州内的很多景点都已经在全国乃至世界享有盛名,如“腾龙洞”、“恩施大峡谷”等;而形成这些奇谷异洞的根本原因与当地的石灰石有关。某中学的“化学兴趣小组”为了测定“腾龙洞”内石灰石样品中CaCO3的含量。取8g样品研碎后放入烧杯中,再加入100g稀盐酸恰好完全反应后,烧杯中剩余物质105.8克(假设样品中杂质不溶也不反应,不考虑水的蒸发及CO2的溶解等因素,结果保留百分号前一位小数)。试计算:
(1)样品中CaCO3的质量分数是多少_________?
(2)所得溶液中溶质的质量分数是多少_________?
62.5% 5.4% 【解析】据质量守恒定律可知,反应前后物质的总质量不变,生成二氧化碳的质量为:8g+100g-105.8=2.2g,设样品中碳酸钙的质量为x,生成氯化钙的质量为y CaCO3 + 2HCl == CaCl2 + H2O + CO2↑ 100 111 44 x y 2.2g 100/x=44/2.2g x=5g 样品中CaCO3的质量分数是5g÷8g...查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com