
分析 (1)根据化合物中各元素质量比=各元素的相对原子质量×原子个数之比;进行解答;
(2)根据相对分子的质量为组成分子的各原子的相对原子质量之和,进行解答;
(3)根据物质中某元素的质量分数=$\frac{该元素的相对原子质量×原子个数}{该物质的相对分子质量}$×100%=$\frac{物质中某元素的质量}{物质的质量}$×100%,进行解答.
解答 解:(1)根据化合物中各元素质量比=各元素的相对原子质量×原子个数之比;可得帕拉米韦中氢元素与氧元素的质量比为:(16×4):(1×28)=16:7;
(2)根据相对分子的质量为组成分子的各原子的相对原子质量之和,帕拉米韦的相对分子量为328,则:12×15+1×28+14x+16×4=328,解得x=4;
(3)根据物质中某元素的质量分数=$\frac{该元素的相对原子质量×原子个数}{该物质的相对分子质量}$×100%,可得帕拉米韦中氧元素的质量分数=$\frac{16×4}{328}$×100%;
根据物质中某元素的质量分数=$\frac{物质中某元素的质量}{物质的质量}$×100%可得,含有氧元素6.4g的帕拉米韦的质量为6.4g÷$\frac{16×4}{328}$×100%=32.8g.
故答案为:
(1)16:7(或64:28); (2)4;(3)32.8
点评 本题考查学生对物质的相对分子的质量、物质中某元素的质量分数,质量比计算方法的理解与应用的能力.


 全优点练单元计划系列答案
全优点练单元计划系列答案科目:初中化学 来源: 题型:解答题

查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
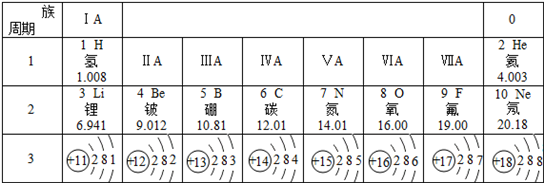
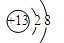 ;与该离子电子层结构相同的带一个单位负电荷的阴离子的符号是F-;
;与该离子电子层结构相同的带一个单位负电荷的阴离子的符号是F-;查看答案和解析>>
科目:初中化学 来源: 题型:解答题

查看答案和解析>>
科目:初中化学 来源: 题型:解答题
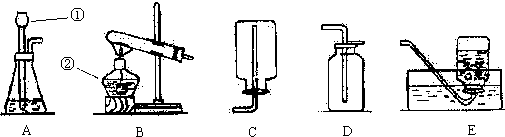
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 根据质量守恒定律,1L氢气和1L氧气反应能生成2L水 | |
| B. | 蜡烛完全燃烧后,蜡烛没有了,这违背了质量守恒定律 | |
| C. | 铁氧气中燃烧,生成四氧化三铁质量等于参加反应的铁丝与氧气的质量之和 | |
| D. | 只有固体、液体间反应遵守质量守恒定律 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com