
 2月7日《自然》杂志消息:中国科技大学的研究人员利用钴和氧化钴混合物的特定的原子排列方法,制得一种可以将CO2转化为液体燃料的电化学催化剂,如图为钴元素在周期表中的信息,下列有关说法错误的是( )
2月7日《自然》杂志消息:中国科技大学的研究人员利用钴和氧化钴混合物的特定的原子排列方法,制得一种可以将CO2转化为液体燃料的电化学催化剂,如图为钴元素在周期表中的信息,下列有关说法错误的是( )| A. | 钴原子的核电核数为27 | |
| B. | CO2转化为液体燃料过程中催化剂质量不变 | |
| C. | 钴是金属元素 | |
| D. | 钴原子的相对原子质量是58.93g |
分析 根据图中元素周期表可以获得的信息:左上角的数字表示原子序数;字母表示该元素的元素符号;中间的汉字表示元素名称;汉字下面的数字表示相对原子质量,结合题干信息进行分析判断即可.
解答 解:A.由元素周期信息可知,钴元素的原子序数为27,则其核电荷数也为27,故正确;
B.催化剂的质量与化学性质在化学反应前后保持不变,故正确;
C.钴的偏旁是“金”字,所以属于金属元素,故正确;
D.根据元素周期表中的一格中获取的信息,可知该元素的相对原子质量为58.93,单位是“1”,通常省略,故错误.
故选D.
点评 本题难度不大,考查学生灵活运用元素周期表中元素的信息及辨别元素种类的方法进行分析解题的能力.


 同步练习强化拓展系列答案
同步练习强化拓展系列答案科目:初中化学 来源: 题型:解答题
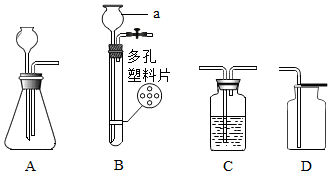 如图是集中实验室制取气体常用的装置,请回答下列问题
如图是集中实验室制取气体常用的装置,请回答下列问题查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| 选项 | 实验目的 | 方案 |
| A | 鉴别羊毛线和棉纱线 | 分别灼烧、闻气味 |
| B | 检验H2中是否混有CH4 | 将气体点燃,观察现象 |
| C | 鉴别氯化铵和氯化钾固体 | 分别取少量固体,加入熟石灰研磨,闻气味 |
| D | 比较石灰水和肥皂水的碱性强弱 | 分别玻璃棒蘸取少量溶液滴到pH标准比色卡对照 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 单质:水、氢气、氧气 | B. | 氧化物:水、二氧化碳、硫酸铜 | ||
| C. | 混合物:煤、石油、冰水共存物 | D. | 还原剂:氢气、碳、一氧化碳 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
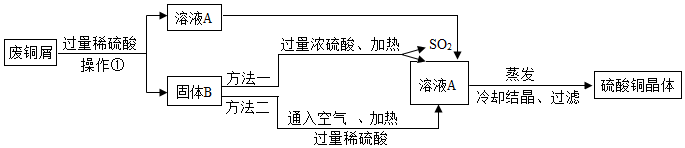
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
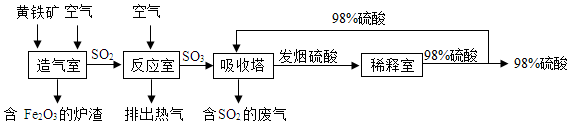
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com