

 ��100%��17g��5%��
��100%��17g��5%��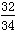 ��100%��
��100%�� Сѧ��ʱ��ѵϵ�д�
Сѧ��ʱ��ѵϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| ���� | ���� | ʵ������ | ���� | |
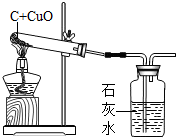
| ̽��һ | ����1��ɫ������̿ | ȡ������Ӧ��ʣ��������������У����ȣ� | �Թ��й���ȫ����� | ����1���� |
| ̽���� | ����2��ɫ����������ͭ | ȡ������Ӧ��ʣ��������Թ��У����Թ��м�������ϡ���� | ��1��_________ ��2��_________ |
����2��������Ӧ�Ļ�ѧ����ʽ��__________�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ��Ķ�����
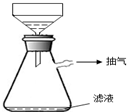 ����ͭ�������������г��������ʣ�������ijѧϰС��չ����̽��ʵ¼��
����ͭ�������������г��������ʣ�������ijѧϰС��չ����̽��ʵ¼��
| ||
| ||
| AlƬ��δ��ĥ�� | AlƬ����ĥ�� | |
| CuSO4��Һ ��5%��5mL�� |
�ޱ仯����Сʱ����Ƭ�ϸ��м������ݣ�������ɫ���� | �������ݣ����ż��ٺ�ɫ���ʣ������ϳ�ʱ�� |
| CuSO4��Һ ��10%��5mL�� |
�ޱ仯����Сʱ����Ƭ�����Զ����ݣ����м��ٺ�ɫ�ߵ� | �Զ����ݣ����ż��٣�����5%����ɫ���ʣ������ϳ�ʱ�� |
| CuCl2��Һ ��5%��5mL�� |
�������ݣ�Ѹ�ٳ��ֺ�ɫ���ʣ��ܿ���Һ�����ɫ�����¶����� | ���������ݣ�Ѹ�ٳ��ֺ�ɫ���ʣ��ܿ���Һ�����ɫ�����¶����� |
| ||
| ||
| ||
| ||
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2009������ʡ�п���ѧ���� ���ͣ�038
ijѧϰС��ͬѧ����ͼ�Լ��еĹ���������Һ��ȡ������ȡ����Һ17 g����������MnO2��ַ�Ӧ��������з��������㣺

(1)С�����ݹ�����������Ԫ�ص������������������������������ʽΪ������������������17 g��5%��![]() ��100%��17 g��5%��
��100%��17 g��5%��![]() ��100%����ʦָ��С���ļ����Ǵ���ģ�����Ϊ�����ԭ����________(����ĸ���)��
��100%����ʦָ��С���ļ����Ǵ���ģ�����Ϊ�����ԭ����________(����ĸ���)��
A�������������Է���������������
B�����������е���Ԫ��û��ȫ��ת�Ƶ�������
(2)������ݻ�ѧ����ʽ������ȡ������������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��������ĩ�� ���ͣ�������

 ��100%
��100%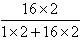 ��100%��3.2g��
��100%��3.2g���鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com