
| A. | ①②③④⑤⑥ | B. | ①② | C. | ①③④⑤ | D. | ③④ |
科目:初中化学 来源: 题型:选择题
| A. | 酒精洒在桌上燃烧时,立即用湿抹布扑盖 | |
| B. | 给试管中的液体加热时,管口不要对着自己或他人 | |
| C. | 家里用剩的汽油倒入下水道里 | |
| D. | 实验用剩的药品放入指定容器内 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
 我们正处在生长发育阶段,需要有充足的营养,如钙的补充.如图是某厂生产的加钙食盐包装标签上的部分文字说明,请仔细阅读并计算:
我们正处在生长发育阶段,需要有充足的营养,如钙的补充.如图是某厂生产的加钙食盐包装标签上的部分文字说明,请仔细阅读并计算:查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 自然沉淀 | B. | 沙一层过滤 | C. | 活性炭吸附 | D. | 杀菌消毒 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
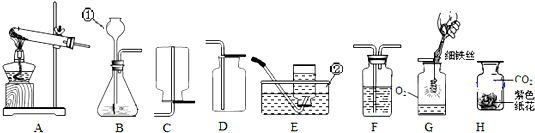
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| 温度/℃ | 20 | 30 | 40 | 50 | |
| 溶解度/g | KCl | 34.0 | 37.0 | 40.0 | 42.6 |
| KNO3 | 31.6 | 45.8 | 63.9 | 85.5 | |
| A. | 20℃时,KCl溶解度大于KNO3的溶解度 | |
| B. | 两物质溶解度相等的温度在20~30℃之间 | |
| C. | 40℃时,5g KCl加10g水可得到15g溶液 | |
| D. | 50℃时,10g KNO3中加20g水,充分溶解后再降温到30℃,有KNO3固体析出 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com