
| 80 |
| 58 |
| x |
| 3.48g |
| 240 |
| 156 |
| y |
| 1.56g |


科目:初中化学 来源: 题型:
| A、测定空气中氧气的含量时,气体减小的体积小于五分之一是红磷过量 |
| B、用高锰酸钾制取氧气并用排水法收集时,水槽中水变红是试口没有放一团棉花 |
| C、做细铁丝在氧气中燃烧的实验时,集气瓶炸裂是集气瓶底没有加水或铺一层细沙 |
| D、用过氧化氢溶液制取氧气并用向上排空气法集时,收集的氧气不能使带火星的木条复燃,是因为氧气中水份含量太高 |
查看答案和解析>>
科目:初中化学 来源: 题型:
| A、HCl和KOH |
| B、Na2CO3和Ba(OH)2 |
| C、HCl和Ca(OH)2 |
| D、Ca(OH)2和H2SO4 |
查看答案和解析>>
科目:初中化学 来源: 题型:
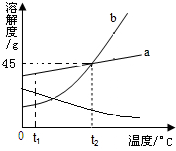 如图是A、B、C三种物质的溶解度曲线,下列说法正确的是( )
如图是A、B、C三种物质的溶解度曲线,下列说法正确的是( )| A、在t2℃时,三种物质溶解度的大小关系是A=B>C |
| B、t2℃时,将50克A加入100g水中,充分溶解后所得溶液的质量为150g |
| C、t2℃时的A、B、C三种物质的饱和溶液分别降温到t1℃,所得溶液溶质质量分数的大小关系是B>C>A |
| D、将等质量t2℃的A、B、C三种饱和溶液分别降温至t1℃,A析出的晶体最多,C没有晶体析出 |
查看答案和解析>>
科目:初中化学 来源: 题型:
查看答案和解析>>
科目:初中化学 来源: 题型:
查看答案和解析>>
科目:初中化学 来源: 题型:
| 序号 | 错误观点 | 否定例证(化学方程式) |
| (1) | 分解反应一定有单质生成 | |
| (2) | 凡有化合物生成的反应都是化合反应 | |
| (3) | 有单质和化合物生成的反应一定是置换反应 | |
| (4) | 有盐和水生成的反应一定是中和反应 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com