
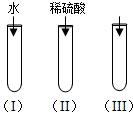
 氧化铜(CuO)是一种黑色固体,可溶于稀硫酸中.某同学想知道是稀硫酸中的H+、H2O和SO42-中的哪种粒子能使氧化铜溶解.请你和他一起通过如图所示三个实验来完成这次探究活动.
氧化铜(CuO)是一种黑色固体,可溶于稀硫酸中.某同学想知道是稀硫酸中的H+、H2O和SO42-中的哪种粒子能使氧化铜溶解.请你和他一起通过如图所示三个实验来完成这次探究活动.分析 (1)稀硫酸中存在三种粒子,即水分子、氢离子、硫酸根离子,据此进行分析解答;
(2)实验I中加入的是水,实验I是验证水能否使氧化铜溶解;
(3)实验I、实验III中的氧化铜不溶解,II中氧化铜溶解,据此进行分析解答;
(4)根据分析得出结论;
(5)根据信息结合现象写出反应的方程式.
解答 解:(1)稀硫酸中存在水分子、氢离子、硫酸根离子,可能是稀硫酸中的水分子、氢离子或硫酸根离子中的一种使氧化铜溶解;故答案为:可能是H+使CuO溶解;可能是SO42-使CuO溶解;
(2)实验I中,氧化铜不溶解,说明水分子不能使氧化铜溶解;故填:①;
(3)因为Ⅰ实验证明了H2O不能使CuO溶解的结论,实验Ⅱ中既有H+,又有SO42-和H2O,其中水分子已经证明了不能使CuO溶解,而且知道实验Ⅱ中的现象是氧化铜溶解,但三个实验必须得出实验结果,如果实验三再加盐酸,那硫酸根就没法证明了,所以实验Ⅲ中应加入的物质应该是含硫酸根的溶液;故填:Na2SO4等;固体不溶解;SO42-;
(4)通过实验可以得知,水分子和硫酸根离子都不能使氧化铜溶解,使氧化铜溶解的是氢离子,只有含有大量氢离子的溶液才可以和氧化铜反应,使之溶解;故填:稀硫酸中的H+使CuO溶解;
(5)因为铜不活泼,所以根据所学知识可以先将铜灼烧变为氧化铜,再用酸溶解,洗涤即可;故反应的方程式分别为:2Cu+O2$\frac{\underline{\;\;△\;\;}}{\;}$2CuO;CuO+H2SO4=CuSO4+H2O.
点评 本题主要考查了酸溶液和氧化铜反应的本质,是溶液中的氢离子和氧化铜反应的结果,培养学生分析问题、解决问题的能力.


 100分闯关期末冲刺系列答案
100分闯关期末冲刺系列答案科目:初中化学 来源: 题型:解答题
| 实验操作 | 实验现象 | 实验结论 |
| ①取少量固体的于试管中,加水振荡制直至完全溶解. | 不产生气泡 | 猜想Ⅰ不成立. |
| ②取少量①的溶液于试管中,滴加过量的Ba(NO3)2溶液. | 产生白色沉淀 | 证明有Na2CO3存在.化学反应方程为:Na2CO3+Ba(NO3)2═BaCO3↓+2NaNO3 |
| ③取少量②的溶液于试管中,滴加无色酚酞试液. | 酚酞试液变红 | 证明NaOH存在. |
| 结合以上实验现象,说明猜想Ⅱ是成立的. | ||
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | FeCl3 NaCl Ba(OH)2 | B. | KCl HCl NaNO3 | ||
| C. | Na2SO4 HCl H2SO4 | D. | CuCl2 NaNO3 K2SO4 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
| 实验操作 |  | 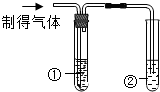 |
| 实验现象 | 澄清石灰水变浑浊 | 试管①澄清石灰水未变浑浊 试管②澄清石灰水变浑浊 |
| 实验结论 | 说明石灰水未变质 | 说明制得的气体中有CO2或二氧化碳气体 |
| 实验操作 | 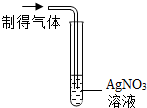 |  |
| 实验现象 | 出现白色沉淀 | 紫色石蕊溶液变红 |
| 实验结论 | 有HCl气体 | 有HCl气体 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 燃烧煤容易造成空气污染,所以应禁止通过燃烧煤来提供能源 | |
| B. | 在煤、石油、天然气等三大化石燃料中,天然气是相对清洁的能源 | |
| C. | 垃圾分类回收既可以充分利用资源又可以减少环境污染 | |
| D. | 用肥皂水区分硬水和软水时,泡沫多的是软水,泡沫少的是硬水 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
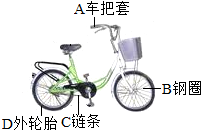 化学与生活和生产密切相关:
化学与生活和生产密切相关:查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com