
【题目】小明同学为了配制一定质量分数的氢氧化钠溶液,进行的实验操作如下图所示,有关该同学的实验说法正确的是
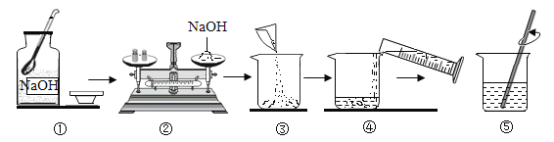
A.称量时,需先取药品再放砝码和调节游码使天平平衡
B.小明同学的实验操作中错误之处有两处
C.该实验操作过程中还需用到胶头滴管
D.量筒量取水时,若仰视读数会导致实验结果偏大
 小学期末冲刺100分系列答案
小学期末冲刺100分系列答案 期末复习检测系列答案
期末复习检测系列答案 超能学典单元期中期末专题冲刺100分系列答案
超能学典单元期中期末专题冲刺100分系列答案 黄冈360度定制密卷系列答案
黄冈360度定制密卷系列答案科目:初中化学 来源: 题型:
【题目】下列图像不能正确反映对应变化关系的是 ( )
A.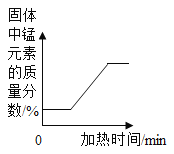 加热一定质量的高锰酸钾
加热一定质量的高锰酸钾
B.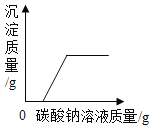 向含有一定量HCl和CaCl2的溶液中滴加Na2CO3溶液
向含有一定量HCl和CaCl2的溶液中滴加Na2CO3溶液
C.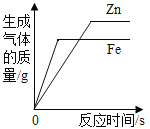 常温下,相同质量的锌和铁分别与足量的溶质质量分数相同的稀硫酸反应
常温下,相同质量的锌和铁分别与足量的溶质质量分数相同的稀硫酸反应
D.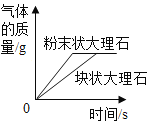 向两份质量相同的块状大理石和粉末状大理石中,分别加入足量的等浓度的稀盐酸
向两份质量相同的块状大理石和粉末状大理石中,分别加入足量的等浓度的稀盐酸
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】某K2CO3样品,可能含有Na2CO3、NaHCO3、CuCl2、NaCl中的几种杂质。取该样品6.9g,加入50g稀盐酸中,恰好完全反应得到无色溶液,同时产生2.2g气体。下列判断正确的是( )
A.反应后得到无色溶液,说明样品中一定没有CuCl2
B.NaCl不与盐酸反应,说明样品中一定没有NaCl
C.所加稀盐酸中溶质的质量分数为3.65%≤w≤7.3%
D.Na2CO3和NaHCO3都能和稀盐酸反应生成气体,说明样品中Na2CO3和NaHCO3至少有一种
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】胃酸过多须服用抗酸药物(能与盐酸反应),常用的抗酸药物有碳酸氢钠片、铝碳酸镁片,兴趣小组的同学对这两种药物开展如下探究。
(查阅资料)①铝碳酸镁片的主要成分的化学式为AlMg(OH)3CO3;
②抗酸原理:抗酸药物中的离子和胃酸中的氢离子反应,降低胃液酸性。
活动一:定性探究抗酸药物与“胃酸”的反应。
(1)铝碳酸镁片中含有铝离子、镁离子、氢氧根离子和碳酸根离子。结合上述知识分析,该药物起抗酸作用的微粒是_____(填化学符号)。
(2)小王取一定量碳酸氢钠片与4mLpH═1的稀盐酸(模拟胃酸)反应。药片中其他成分不溶于水也不参加反应。他对反应后溶液的成分产生了兴趣。
(作出猜想)
猜想 1:只含 NaCl;
猜想 2:_____;
猜想 3:NaCl、NaHCO3
(设计实验)
实验步骤 | 实验现象 | 实验结论 | |
实验一 | 取一定量反应后的溶液于试管中,滴加_____ | 无明显现象 | 猜想 3错误 |
实验二 | 另取一定量反应后的溶液于试管中,______ | ______ | 猜想 2正确 |
实验二中涉及反应的化学方程式为______。
活动二:定量探究抗酸药物与“胃酸”的反应,对比分析产生 CO2的速率快慢和中和酸的能力强弱。
如图 1,利用数字化实验分别测定碳酸氢钠片、铝碳酸镁片与“胃酸”反应时,产生 CO2的速率快慢和 pH的变化,得到“二氧化碳浓度与时间”曲线(如图 2)、“pH与时间”曲线(如图 3)。
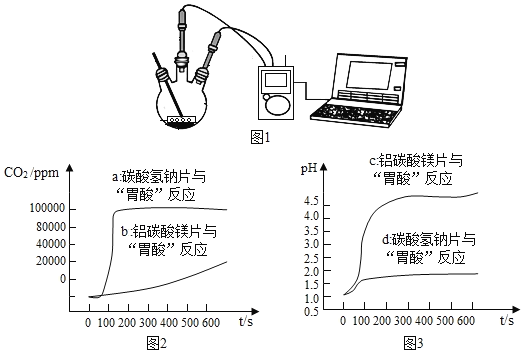
(1)服用碳酸氢钠片更易造成胃胀气,原因是_____。
(2)铝碳酸镁片中和酸的能力更强,理由是_____。
(反思与提升)日常生活中,我们应该根据个人的具体病情,选择合适种类的胃药。
查看答案和解析>>
科目:初中化学 来源: 题型:
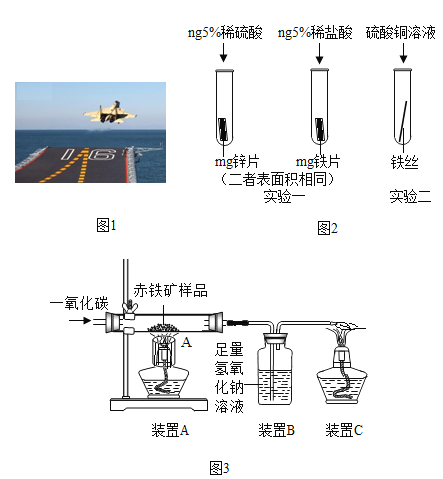
【题目】金属材料在国防建设中起着重要的作用,图1为歼﹣15飞机在辽宁舰上起飞.
(1)铝合金用于制造飞机的外壳,铝合金材质的主要优点是______(写出一点即可).
(2)改装前的辽宁舰舰身锈迹斑斑,钢铁的锈蚀主要是铁与空气中的_______共同作用的结果.工业生产中常用稀盐酸除去铁制品表面的铁锈,该反应的化学方程式为______.
(3)为了避免轮船的钢质外壳被腐蚀,通常在轮船外壳上镶嵌比铁活动性强金属.小明为探究锌、铁、铜三种金属的活动性顺序,设计了如图2的两个实验:
①实验一中,小明以“金属表面产生气泡的快慢”为标准来判断锌、铁的活动性强弱,有同学认为不够合理,理由是_______.
②实验二中,若出现__现象,可证明铁的活动性强于铜,该反应的化学方程式为__.
(4)辽宁舰的建造耗费了大量的钢材.某兴趣小组在实验室用图3所示装置模拟炼铁的化学原理,并测定赤铁矿中氧化铁的质量分数(装置气密性良好,反应完全且赤铁矿中的杂质不参加反应,称重赤铁矿样品的质量为wg).
①装置B中发生反应的化学方程式为____.
②要测定该赤铁矿样品中氧化铁的质量分数,需要测量的数据是__或__.
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】图I中 A、B、C、D、E 为中学常见的物质,其中 A 为含钠元素的化合物,D 的相对分子质量为 100,E 溶液为无色,它们的相互转化的关系如图Ⅰ所示。小玉同学测得D 与稀盐酸反应后的溶液 pH 为 2,向适量该溶液中逐滴加入碳酸钠溶液,并测得溶液的 pH随加入碳酸钠溶液体积的变化曲线如图Ⅱ所示(此处的 A、B、C、D 均为曲线上的点),请回答下列问题:
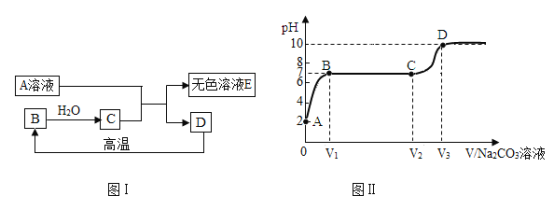
请填写下列空白
(1)A:_____ C:_____
(2)图Ⅱ中,A 点处溶液中含有的主要离子有_____(写离子符号);
(3)BC 段发生反应的化学方程式是________________;
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】(1)三大化石燃料是指煤、____________和天然气,它们都是不可再生能源。天然气的主要成分是甲烷,其燃烧的化学方程式为_______________.
(2)可燃物燃烧的条件之一是____________________(任写一条即可,下一空同样),灭火的原理就是任意破坏一个燃烧的条件,所以生活中扑灭油锅着火的方法有______________________。
(3)水蒸气与炽热的炭反应可生成一氧化碳和氢气,其反应的化学方程式为:________,基本反应类型是________________.
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】如图是初中化学中常见物质间的转化关系。其中,在通常情况下,C为胃酸的主要成份,E是生活中常用的调味品,F、G是组成元素相同的两种气体,Q、R都是黑色固体(部分反应条件略去),试回答下列问题:
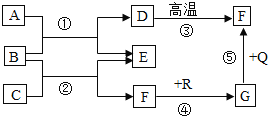
(1)C的化学式为_________,D的一种用途为________。
(2)反应②的化学方程式为________。
(3)上述5个反应中共涉及_______种基本反应类型。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】t℃时,在100g质量分数为20%的KNO3不饱和溶液甲中加入10gKNO3固体,恰好得到饱和溶液乙。下列说法正确的是
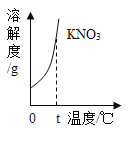
A.t℃时,KNO3 的溶解度为30g
B.乙溶液的质量分数为30%
C.适当降低温度,可以使甲溶液变成饱和溶液
D.升高温度,甲、乙两溶液的质量分数都增大
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com