
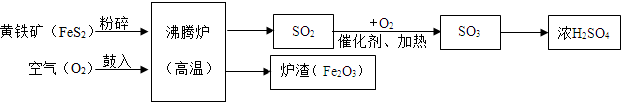
���� ��1�����ݽ������˳�����ݽ��з�����ɣ�
��2���ٸ��ݽ�����������������Ԫ����ɣ�һ��Ԫ������Ԫ�أ���һ��Ԫ���ǽ���Ԫ�ط����жϣ�
�ڸ��ݻ�������������Ӧ��ĽӴ�����ӿ췴Ӧ�ٶȽ��з�����
�۸������е������ҳ���Ӧ��������Լ���Ӧ������Ȼ�����������غ㶨����д��ѧ����ʽ��
�ܸ���Ũ����ʹ�õ�ע����������ش�
��3�����ݷϸ����õ��������ÿ��Խ�Լ��Դ�����жϣ�
��4���������������ᷴӦ�ų����������ش�
��� �⣺��1�������������˳��ΪK��Ca��Na��Mg��Al��Zn��Fe��Sn��Pb����H����Cu��Hg��Ag��Pt��Au�������ŵ�������ý������������ǿ���������ݽ������˳���֪��������ͭ����������Լ�������Ӧ������λ�������һλ�������÷��Ͻ������˳��
��2����ͨ��������Ӧ�����е����ʿ�֪����������������������Ԫ����ɣ�һ��Ԫ������Ԫ�أ���һ��Ԫ������Ԫ�أ����ڽ��������
�ڷ�Ӧ��Ӵ����Խ��ӦԽ���ң���������������Ӧ��ĽӴ�������ӿ췴Ӧ�ٶȣ����Խ���������飬Ŀ���ǣ�����Ӧ��ĽӴ�������ӿ췴Ӧ�����ʣ�
��¯����Fe2O3���ڹ�ҵ�Ͽ����������䷴Ӧ��ԭ���ǣ�Fe2O3+3CO$\frac{\underline{\;����\;}}{\;}$2Fe+3CO2��
��Ũ������и�ʴ�ԣ�ϡ��Ũ����ʱ��С�Ľ��ὦ�������ϣ�Ӧ�����ô�����ˮ��ϴ����Ϳ3%-5%��̼��������Һ��
��3��Ŀǰ����������50%���ϵķϸ����õ��������ã���Ŀ���ǽ�Լ������Դ����������ɿ����ֹ���������أ�
��4����Ҳ�������⣬��ԭ������������е� ��ͬ���õĽ�������������Ʒ����ʢ�й���ϡ�����ϴ���У��۲쵽��Һ��ƣ�����ɫ�����ݳ���д�����в����������������ᷴӦ�������̻���������������Ӧ�Ļ�ѧ����ʽ�ǣ�Fe+2HCl�TFeCl2+H2�����䷴Ӧ�������û���Ӧ��
�ʴ�Ϊ����1��Fe����2������������������Ӧ��ĽӴ�������ӿ췴Ӧ�����ʣ���Fe2O3+3CO$\frac{\underline{\;����\;}}{\;}$2Fe+3CO2�����ô�����ˮ��ϴ����3��A����4��Fe+2HCl�TFeCl2+H2�����û���Ӧ��
���� �����ѶȲ��Ǻܴ����ս������˳������������������;�Ȳ��������������ȷ�����Ĺؼ����ڣ�



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ������Ԫ����� | |
| B�� | ��������Ԫ����̼Ԫ�� | |
| C�� | �������г��ȼ�տ��������ж���������Cl2�� | |
| D�� | ���ж��Ե����� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | �Ȼ��ƺͶ�����̼�����ɷ��ӹ��ɵ� | |
| B�� | ͬ��Ԫ����ɵ����ʲ�һ���ǵ��� | |
| C�� | ����һ���ܼӿ컯ѧ��Ӧ���� | |
| D�� | �����κ�ˮ�ķ�Ӧһ�����кͷ�Ӧ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | KMnO4��K2MnO4 | B�� | SO3��H2SO4 | C�� | Cu��OH��2��NaOH | D�� | KClO3��KCl |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com