
| A. | SO2和SO3 | B. | H2S和SO3 | C. | H2S和H2S03 | D. | Na2SO4和SO3 |
分析 根据在化合物中正负化合价代数和为零,结合各选项中的化学式进行解答即可.
解答 解:A、氧元素显-2价,设SO2和SO3中硫元素的化合价分别是x、y,根据在化合物中正负化合价代数和为零,x+(-2)×2=0,则x=+4价;y+(-2)×3=0,则y=+6价;故选项错误.
B、氢元素显+1价,氧元素显-2价,设H2S和SO3中硫元素的化合价分别是x、y,根据在化合物中正负化合价代数和为零,(+1)×2+x=0,则x=-2价;y+(-2)×3=0,则y=+6价;故选项错误.
C、氢元素显+1价,氧元素显-2价,设H2S和H2S03中硫元素的化合价分别是x、y,根据在化合物中正负化合价代数和为零,(+1)×2+x=0,则x=-2价;(+1)×2+y+(-2)×3=0,则y=+4价;故选项错误.
D、钠元素显+1价,氧元素显-2价,设Na2SO3和SO3中硫元素的化合价分别是x、y,根据在化合物中正负化合价代数和为零,(+1)×2+x+(-2)×4=0,则x=+6价;y+(-2)×3=0,则y=+6价;硫元素的化合价均为+6价,故选项正确.
故选:D.
点评 本题难度不大,掌握利用化合价的原则(化合物中正负化合价代数和为零)计算指定元素的化合价的方法即可正确解答此类题.


 轻松夺冠全能掌控卷系列答案
轻松夺冠全能掌控卷系列答案科目:初中化学 来源: 题型:选择题
| A. | 青蒿素由碳、氢、氧三个元素组成 | |
| B. | 青蒿素中碳、氧元素的质量比为3:1 | |
| C. | 青蒿素由碳原子、氢原子和氧原子构成 | |
| D. | 青蒿素中氢元素的质量分数最小 |
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
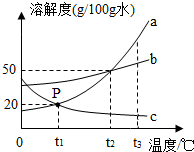 水是生命的源泉,也是不可缺少的资源.
水是生命的源泉,也是不可缺少的资源.| 成分 | Ca | K | Zn | F |
| 含量(mg/L) | 20 | 3 | 0.06 | 0.02 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 绿色化学的核心是利用化学原理从源头上减少和消除工业生产 | |
| B. | 用氢氧化镁代替氢氧化铝中和过多胃酸 | |
| C. | 人体缺乏维生素A会引起夜盲症 | |
| D. | 日常生活中使用的有机玻璃、睛纶、蚕丝等都属于合成纤维 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
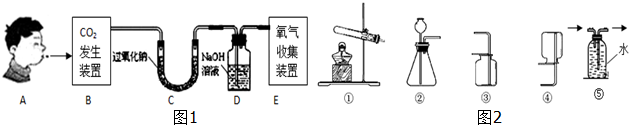
| 实验步骤 | 实验现象 | 实验结论 |
| 将CO2与Na2O2反应后的固体取少量于试管中,加入稀盐酸(或稀硫酸等),把产生的气体通入足量的澄清石灰水中 | ①有大量气泡产生 ②澄清石灰水变浑浊 | 猜想③是正确的 |
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
 铝是目前人们在生产、生活中使用较多的一种金属.
铝是目前人们在生产、生活中使用较多的一种金属.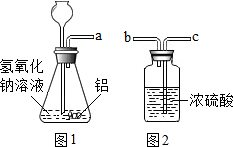
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
| 实验步骤 | 实验现象 | 分析与结论 |
| ①在盛有少量蒸馏水的烧杯中滴入2~3滴石蕊试液 | 液体显紫色 | 结论:蒸馏水不能使酚酞变红 |
| ②在步骤①的烧杯中再滴加浓盐酸 | 试液变红 | 结论:酸性溶液能使紫色石蕊试液变红 |
| ③按图甲所示进行实验 | 烧杯B中试液变红 | 原因:由于浓盐酸具有较强的挥发性,所以倒扣的烧杯中会有大量的氯化氢分子存在,这些氯化氢的分子溶于烧杯B中会使该溶液变为稀盐酸而呈酸性,所以烧杯B中的紫色石蕊会变为红色, 结论:分子是不断运动的 |
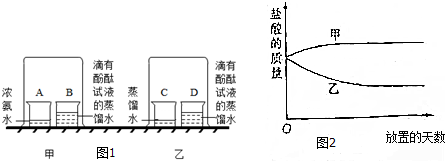
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com