
科目:初中化学 来源: 题型:解答题

| 物质 | NaCl | NaOH | Na2CO3 | NaHCO3 |
| 常温下的溶解度/g | 36 | 109 | 21.5 | 9.6 |
| 常温下某稀溶液的pH | 7 | 13 | 11 | 9 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
 茶,是一片树叶的故事.绿茶中的单宁酸【C76H52O46】具有抑制血压上升、清热解毒、抗癌等功效.下列说法正确的是( )
茶,是一片树叶的故事.绿茶中的单宁酸【C76H52O46】具有抑制血压上升、清热解毒、抗癌等功效.下列说法正确的是( )| A. | 一个单宁酸分子中含23个O2 | |
| B. | 单宁酸分子是由碳、氢、氧三种元素组成 | |
| C. | 单宁酸分子中碳、氢、氧原子个数比为38:26:23 | |
| D. | 单宁酸由76个碳原子、52个氢原子和46个氧原子构成 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
 人体中钙元素主要存在牙齿和骨骼中,以羟基磷酸钙[Ca10(PO4)6(OH)2]形式存在,其相对分子质量为1004,如图是小宇同学收集的纯牛奶的包装说明.阅读答题:
人体中钙元素主要存在牙齿和骨骼中,以羟基磷酸钙[Ca10(PO4)6(OH)2]形式存在,其相对分子质量为1004,如图是小宇同学收集的纯牛奶的包装说明.阅读答题:查看答案和解析>>
科目:初中化学 来源: 题型:多选题
| A. | K2CO3 | B. | NaHCO3 | C. | MgCO3 | D. | BaCO3 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:多选题
| A. | 原子的质量几乎都集中在原子核上 | |
| B. | 原子通过得失电子形成离子,但离子不能形成原子 | |
| C. | 原子、分子、离子、电子都是构成物质的微粒 | |
| D. | 由分子构成的物质发生化学变化时,分子本身改变 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
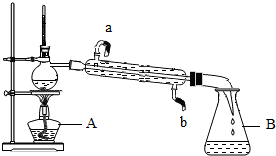 (1)实验室用的蒸馏水可以通过蒸馏自来水来制取.操作方法是:在如图所示蒸馏烧瓶中加入约$\frac{1}{3}$体积的自来水,再加入几粒沸石(或碎瓷片).在确定各连接部位严密不漏气后,加热蒸馏烧瓶,注意不要使液体沸腾得太剧烈.弃去开始馏出的部分液体,收集到10mL左右蒸馏水后,停止加热.请回答下列问题:
(1)实验室用的蒸馏水可以通过蒸馏自来水来制取.操作方法是:在如图所示蒸馏烧瓶中加入约$\frac{1}{3}$体积的自来水,再加入几粒沸石(或碎瓷片).在确定各连接部位严密不漏气后,加热蒸馏烧瓶,注意不要使液体沸腾得太剧烈.弃去开始馏出的部分液体,收集到10mL左右蒸馏水后,停止加热.请回答下列问题:
| 实验编号 | 1 | 2 |
| 反应物 | 5%H2O2 | 5%H2O2 |
| 催化剂 | 1g水泥块 | 1gMnO2 |
| 时间 | 165秒 | 46秒 |
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
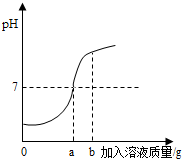 用质量分数为5%的稀盐酸和10%的氢氧化钠溶液进行中和反应实验时,反应过程中溶液的酸碱度变化如下图所示:
用质量分数为5%的稀盐酸和10%的氢氧化钠溶液进行中和反应实验时,反应过程中溶液的酸碱度变化如下图所示:查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com