
分析 根据氢气的质量可以计算单质镁的质量,从而可以计算出镁带中单质镁的质量,从而求出变成MgO的质量,利用化合物中元素=化合物的质量×元素的质量分数解答.
解答 解:设镁带中单质镁的质量为x.
Mg+2HCl=MgCl2+H2↑
24 2
x 0.4g
$\frac{24}{2}$=$\frac{x}{0.4g}$
x=4.8g
mMgO=5g-4.8g=0.2g
∴m已变质Mg=0.2g×$\frac{24}{24+16}$×100%=0.12g
∴mMg总=4.8g+0.12g=4.92g
答:镁带在变质前的质量为4.92 g.
点评 根据化学方程式计算时,第一要正确书写化学方程式,第二要使用正确的数据,第三计算过程要完整.


 开心快乐假期作业暑假作业西安出版社系列答案
开心快乐假期作业暑假作业西安出版社系列答案 名题训练系列答案
名题训练系列答案 期末集结号系列答案
期末集结号系列答案科目:初中化学 来源: 题型:实验探究题

| 物质 | NaCl | NaOH | Na2CO3 | NaHCO3 |
| 溶解度g | 36 | 109 | 215 | 9.6 |
| 操作步骤 | 实验现象 | 结论及化学方程式 |
| 取样于试管中, 滴加足量的稀盐酸 | 有气泡产生 | 该溶液是Na2CO3 相关的化学方程式Na2CO3+2HCl=2NaCl+H2O+CO2↑ |
| 实验步骤 | 实验现象 | 实验结论 |
| a.取少量该溶液于一支试管中,加入足量 CaCl2或BaCl2 | 有白色沉淀产生 | 该氢氧化钠溶液已变质 |
| b.将步骤a所得的液体静置,取上层清液于另一支试管中,滴加无色酚酞(或CuSO4溶液) | 酚酞变红(或产生蓝色沉淀) | 该氢氧化钠溶液已部分变质 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
| 实验 | 水的体积 | 所加物质 | 测量液体温度(℃) |
| 实验1 | 50mL | NH4Cl | 15 |
| 实验2 | 50mL | CaCl2 | 28 |
| 实验3 | 50mL | NaCl | 21 |
| 实验4 | 50mL | 无 | 22 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
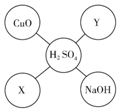 对知识的及时整理与归纳是学习科学的重要方法.某同学在学习了硫酸的化学性质后,初步归纳出稀硫酸与其他物质相互反应的关系,如图所示(“-”表示相连的两种物质能发生反应,五个圈中的物质属于不同的类别).
对知识的及时整理与归纳是学习科学的重要方法.某同学在学习了硫酸的化学性质后,初步归纳出稀硫酸与其他物质相互反应的关系,如图所示(“-”表示相连的两种物质能发生反应,五个圈中的物质属于不同的类别).查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
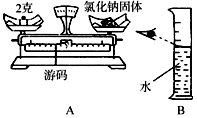 实验室欲配制100克溶质质量分数为10%的氯化钠溶液,请回答下列问题:
实验室欲配制100克溶质质量分数为10%的氯化钠溶液,请回答下列问题:查看答案和解析>>
科目:初中化学 来源: 题型:计算题
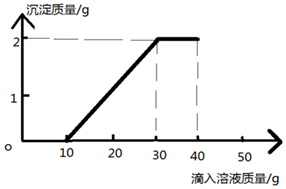 某班同学完成制取二氧化碳的实验后,对回收的盐酸和氯化钙混合溶液(不考虑其他杂质)进行了以下实验:取62.44g该混合溶液于烧杯中,向烧杯中滴入溶质质量分数
某班同学完成制取二氧化碳的实验后,对回收的盐酸和氯化钙混合溶液(不考虑其他杂质)进行了以下实验:取62.44g该混合溶液于烧杯中,向烧杯中滴入溶质质量分数查看答案和解析>>
科目:初中化学 来源: 题型:计算题
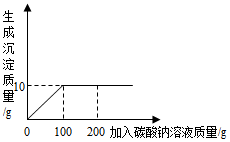 为测定由氯化钙和氯化钠组成的固体样品中氯化钙的含量,某同学进行了如下实验:
为测定由氯化钙和氯化钠组成的固体样品中氯化钙的含量,某同学进行了如下实验:查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 10m克 | B. | 24m克 | C. | 80m克 | D. | $\frac{1000a}{(100-a)}$克 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com