
【题目】(1)下表是生活饮用水国家标准的部分内容。
生活饮用水水质常规检验项目及限值(部分)
项目 | 限值 |
色度 | 不超过15度,并不得呈现其他异色 |
浑浊度 | 不超过1度,特殊情况下不超过5度 |
pH | 6.5~8.5 |
总硬度(以CaCO3计) | 450mg/L |
铝 | 0.2mg/L |
铁 | 0.3mg/L |
硫酸盐 | 250mg/L |
①上表中“铝”指的是_______(选填“单质”“元素”或“原子”)。
②生活中硬水软化的方法是___________。
③Cl2、ClO2均可作自来水消毒剂,其中氯元素的化合价分别是____________。
④1L合格的生活饮用水中,均以CaCO3计算硬度,则钙元素的含量不超过_____mg/L。
⑤实验室用上述水样通电分解,产生氢气和氧气的体积比约为______;反应的化学方程式为______。
(2)元素周期表是学习化学的重要工具。下面是元素周期表中1~18号元素原子核外电子排布:
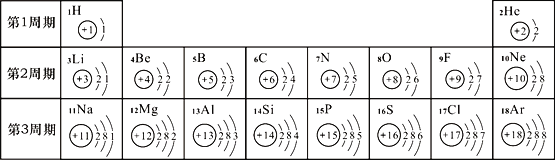
请回答下列问题:
①第17号元素属于______元素(填“金属”或“非金属”),其次外层电子数为______。
②元素的化学性质与原子结构中的_____数关系密切;在同一族中,各元素的原子结构呈现的规律有____(任写一点)。
③地壳中含量最多的金属元素与含量最多的非金属元素组成的化合物为____________。第16号元素在化学反应中容易形成________(填离子符号),该元素的单质在氧气中燃烧的现象是_______________。
【答案】元素 煮沸 0价、+4价 180 2:1 2H2O![]() 2H2↑+O2↑ 非金属 8 最外层电子 最外层电子数相等或由上而下电子层数依次递增 氧化铝 S2- 剧烈燃烧,发出明亮的蓝紫色火焰,产生有刺激性气味的气体
2H2↑+O2↑ 非金属 8 最外层电子 最外层电子数相等或由上而下电子层数依次递增 氧化铝 S2- 剧烈燃烧,发出明亮的蓝紫色火焰,产生有刺激性气味的气体
【解析】
(1)①上表中“铝”指的是元素;
②生活中硬水软化方法是加热煮沸,在实验室中是蒸馏;
③Cl2、ClO2均可作自来水消毒剂,其中氯元素的化合价分别是:0价、+4价;
④1L合格的生活饮用水中,均以CaCO3计算硬度,则钙元素的含量不超过:450mg×![]() =180mg;
=180mg;
⑤实验室用上述水样通电分解,生成氢气和氧气,2H2O![]() 2H2↑+O2↑;其中氢气和氧气的体积比是2:1;
2H2↑+O2↑;其中氢气和氧气的体积比是2:1;
(2)①第17号元素是氯元素,氯元素属于非金属元素,其次外层电子数为8;
②元素的化学性质与原子结构中的最外层电子数关系密切;在同一族中,各元素的原子结构呈现的规律有:最外层电子数相等,由上而下电子层数依次递增;
③地壳中含量最多的金属元素是铝元素,与含量最多的非金属元素--氧元素组成的化合物为氧化铝;第16号元素是硫元素,硫原子最外层电子数是6,在化学反应中容易得到2个电子形成带2个单位负电荷的S2-;硫在氧气中燃烧的现象是剧烈燃烧,发出明亮的蓝紫色火焰,产生有刺激性气味的气体。


科目:初中化学 来源: 题型:
【题目】木炭和一氧化碳还原氧化铜的实验装置分别如图甲和图乙所示,下列说法错误的是( )
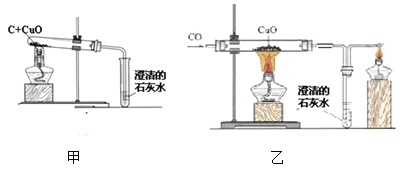
A. 实验时都可以观察到黑色粉末变红,澄清石灰水变浑浊
B. 两个实验的相关反应中,只有碳元素化合价发生了改变
C. 乙装置中应当先通 CO,后点燃玻璃管下的酒精灯,防止发生爆炸
D. 乙装置最右端放一酒精灯的目的是处理未反应的 CO,防止污染空气
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】A~K是初中化学常见物质,它们之间的转化关系如图所示(反应条件已略去).其中B是红棕色固体,G为红色固体,A、E为气体:
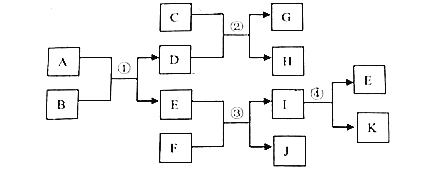
请回答下列问题
(1)请写出以下物质的化学式:F________;G__________.
(2)化合物H中所含金属元素呈现的化合价为_________。
(3)反应①的化学方程式为______________________________。
(4)反应④的化学方程式为_______________________________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】食盐是生产生活中常见的物质,有着广泛的用途。
(1)海水中含有较多的氯化钠,用海水晒盐可以获得食盐。氯化钠在海水中的存在形式是 _____(填化学符号)。
(2)海水晒盐制得的粗盐中含有一些泥沙,除去泥沙等难溶性杂质以获得较纯净氯化钠的实验方案为:先将粗盐溶于一定量的水中,____________。
(3)现要配制100 g溶质质量分数为2%的食盐水,配制的实验步骤可以概括为计算、称量、_______、转移及贴标签。经计算可知,应用托盘天平称取_______g氯化钠,应选用规格为_________mL的量筒来量取水。
(4)实验室里有两个失去标签的试剂瓶,一瓶装有食盐水,一瓶装有蒸馏水,请写出两种方法来区别它们(要说明结论):①________;②__________。
(5)医疗使用的生理盐水的溶质质量分数约为0. 9%。若要配制500 g 0. 9%的生理盐水,则需要用_____g溶质质量分数为2%的食盐水来稀释。
(6)工业上用电解饱和食盐水的方法来生产烧碱(NaOH)和氯气(Cl2 ),同时还得到另一种单质气体,写出该反应的化学方程式:_______。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】通过分析实验结果推断物质的组成是认识物质的一种方法。研究水的组成就是利用了这种方法。电解水实验结果如图所示:
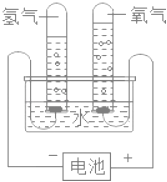
(1)经检验,电解水只生成了氢气和氧气,确定了水是由_____和_____组成的结论,得出此结论的依据是_____。
(2)已知相同状况下,相同体积的任何气体具有相同数目的分子。由于电解水时生成氢气和氧气的体积比为2:1,推求出水分子中_____和_____的个数比为2:1,经进一步科学确认,得出水的化学式为H2O。
(3)电解水的化学方程式为_____;该反应中生成的氢气和氧气的质量比为_____。
(4)相同条件下,氢气和氧气在水中的溶解能力是不相同的,每100g水中最多可以溶解气体的质量如下:
气 体 | 氢 气 | 氧 气 |
每100g水中最多可以溶解气体的质量 | 1.63×10﹣3g | 4.34×10﹣3g |
则相对更易溶于水的气体是_____;由此你认为在水的电解过程中,生成氢气、氧气的体积比可能_____2:1(填“大于”或“小于”)。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】以下是1-18号元素原子最外层电子数与原子核电荷数的关系图,请认真细读后回答:
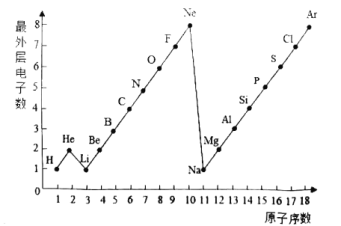
(1)17号元素的最外层电子数为________________.
(2)12号元素与17号元素化合所组成的物质的化学式为__________.
(3)通过上图你发现哪些规律?请写出其中一个_____________.
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】(1)某物质在空气中完全燃烧,生成CO2和H2O,则该物质中一定含有_______元素(填元素符号)。
(2)烹饪鱼时通常将鱼煎过后,再加少许食醋和酒,这是因为它们可以反应生成具有特殊香味的乙酸乙酯(化学式为C4H8O2),每个乙酸乙酯分子是由_______个原子构成的,乙酸乙酯的相对分子质量是_______;在乙酸乙酯中碳元素和氧元素的最简质量比是_______;17.6g乙酸乙酯中所含氧元素的质量为_______g。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】工业生产氟化钠(NaF)的主要流程如下(整个过程中水不参加反应):
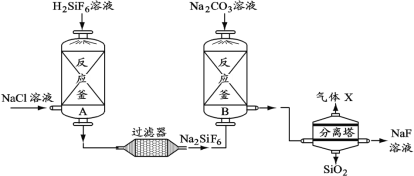
(1)H2SiF6中氟元素(F)的化合价为-1,则硅元素(Si)的化合价为_______;
(2)产物气体X是初中化学常见气体,其组成元素为_______(填元素符号);
(3)产物NaF中的钠元素来自于原料中的_______(填物质的化学式)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com