
| ���� | Ca��ClO3��2 | CaCl2 | KClO3 | KCl |
| �ܽ��/g | 209.0 | 74.5 | 7.3 | 34.2 |
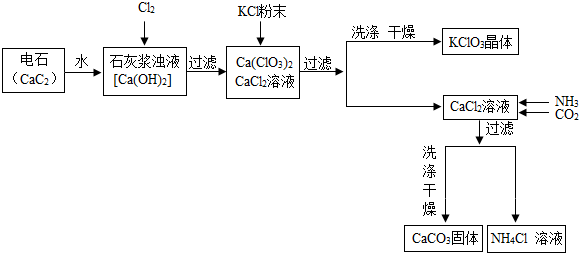
���� ��1�������������ʺ������غ㶨�ɲ�ȫ��ѧ����ʽ��
��2������ͼ�з�Ӧ���̣��ж��ҳ������Ȼ��ط�Ӧ��������ص����ʣ�����ͼ��������Ϣ������ص��ܽ�Ƚ��з������
��3����������������Ӧ�����������д��ѧ����ʽ��
��� �⣺��1�����������غ㶨�ɣ���ѧ��Ӧǰ��ԭ�ӵ���������Ŀ�����ж���һ����������ˮ�����C2H2��
��2����ͼ�з�Ӧ�����Ȼ��ؼ��뵽�Ȼ��ƺ�����ƻ�����з�����Ӧ�����ݸ��ֽⷴӦ�������������Ȼ������Ȼ��ز���Ӧ�����Ȼ���ֻ��������Ʒ�Ӧ��������أ������������ڳ����µ��ܽ�ȱ������ݷ�������ص��ܽ�Ƚ�С����������������ڳ�����������ܽ�Ƚ�С�����Թ���������ػ�ᾧ���������Ca��ClO3��2���ڳ���������ص��ܽ�Ƚ�С�����ɵ�����ع�����ᾧ������
��3����������Ϣ�жϷ�Ӧ����NH3��CO2��CaCl2��Һ����������CaCO3�����NH4Cl��Һ����Ӧ�Ļ�ѧ����ʽΪ��H2O+2NH3+CO2+CaCl2=CaCO3��+2NH4Cl��
���� �����ۺϿ������ʵ��ת�����Ʊ������������غ㶨�ɺ���ȷ��д��ѧ����ʽ�ķ����ǽ���Ĺؼ���



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ʵ��̽����

| ���� | ʵ��ҩƷ | ��Ӧ���� | ������������ |
| H2S | ������������ϡ���� | ������� | ��ɫ���ܶȱȿ���������ˮ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ʵ��̽����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������

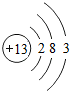 ����ԭ���ڻ�ѧ��Ӧ����ʧ����á���ʧ�������ӣ��γɵ����ӷ���ΪAl3+ͭ��ϡ�����Ӧ����Ũ������һ�������¿��Է�Ӧ���仯ѧ����ʽΪ��Cu+2H2SO4��Ũ��$\frac{\underline{\;\;��\;\;}}{\;}$CuSO4+X��+2H2O����X�Ļ�ѧʽΪSO2��
����ԭ���ڻ�ѧ��Ӧ����ʧ����á���ʧ�������ӣ��γɵ����ӷ���ΪAl3+ͭ��ϡ�����Ӧ����Ũ������һ�������¿��Է�Ӧ���仯ѧ����ʽΪ��Cu+2H2SO4��Ũ��$\frac{\underline{\;\;��\;\;}}{\;}$CuSO4+X��+2H2O����X�Ļ�ѧʽΪSO2���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ��ƶ���
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ��ͭ����������ʹ�õĺϽ� | |
| B�� | ȱ�ƻ������������ | |
| C�� | ������ѧ����������һ����ȷ����������������͵�����ɵ� | |
| D�� | ����ɫ��Ⱦ����ָ��ɫ�������������������Ⱦ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ��ϡ��Ũ���ᡱʵ���У�����ϡ�͵õ���������Һת�����Լ�ƿ�� | |
| B�� | �����εij����ᴿ��ʵ���У�����ʱ������Һֱ�ӵ���©���� | |
| C�� | ������һ�����������������Ȼ�����Һ��ʵ���У�ҩ���ж����ҩƷӦ�Ż�ԭƿ | |
| D�� | �����������ȡ������ʵ���У��ռ��������Ӧ�Ƚ������Ƴ�ˮ����ֹͣ���� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������

�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com