
| A. | 浓硫酸 | B. | 浓盐酸 | C. | 食盐 | D. | 氢氧化钙固体 |
科目:初中化学 来源: 题型:解答题
| 正常情况下胃液中HCl的质量范围 | 0.2g~0.4g |
| 该患者胃液中HCl的质量 | 1.495g |
| 该患者至少要除去的HCl的质量是 | 1.095g |
查看答案和解析>>
科目:初中化学 来源: 题型:多选题
| A. | 铁片放入硫酸铜溶液中,铁片表面有红色物质析出 | |
| B. | 铁、铜分别放入硝酸银溶液里,溶液颜色均发生变化 | |
| C. | 铜的导电性好作导线,铁导电性差 | |
| D. | 铁、铜分别放入稀硫酸中,铁表面产生气泡,而铜的表面无现象 |
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 氧化钙、熟石灰、CaO | B. | 碳酸氢钠、小苏打、NaHCO3 | ||
| C. | 乙醇、酒精、C2H4O2 | D. | 碳酸铵 碳铵 (NH4)2CO3 |
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:推断题
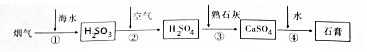
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
| 方法 | 操作 | 现象 | 结论 |
| 1 | 分别取少量A、B溶液于两支试管,分别滴加三滴酚酞溶液 | A溶液不变色 | 是稀硫酸 |
| B溶液变红 | 氢氧化钠溶液 | ||
| 2 | 分别取少量A、B溶液于两支试管,分别滴加少量硫酸铜溶液 | A溶液无明显变化 | 是稀硫酸 |
| B溶液有蓝色絮状沉淀生成 | 氢氧化钠溶液 | ||
| 3 | 分别取少量A、B溶液于两支试管,分别加入碳酸钠溶液 | A溶液中产生气泡 | 是稀硫酸 |
| B溶液中无明显现象 | 氢氧化钠溶液 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com