
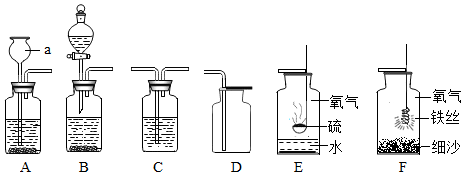
分析 (1)根据实验室常用仪器解答;根据实验室通常用大理石或石灰石和稀盐酸反应制取二氧化碳,反应不需要加热,大理石和石灰石的主要成分是碳酸钙,能和稀盐酸反应生成氯化钙、水和二氧化碳; 不同的实验装置,功能不同;
(2)二氧化硫有毒,是一种污染环境的物质.
(3)在集气瓶中进行燃烧实验时,要注意防止环境污染,防止安全事故的发生.
解答 解:
(1)根据实验室常用仪器可知:a分液漏斗;二氧化碳能够溶于水,不能用排水法收集,密度比空气大,可以用向上排空气法收集,即用D装置收集;
该反应的化学方程式为:CaCO3+2HCl=CaCl2+CO2↑+H2O;
若用C装置代替B装置进行实验,优点为:可以随时控制反应的发生和停止;
(2)硫在氧气中燃烧生成二氧化硫,二氧化硫能和水反应生成亚硫酸,加入水的目的是吸收二氧化硫,防止污染环境.
(3)在“集气瓶中进行燃烧的实验”时应该注意:要防止生成物污染环境,要防止炸裂集气瓶.
答案:
(1)分液漏斗;二氧化碳;CaCO3+2HCl=CaCl2+CO2↑+H2O;可以随时控制反应的发生和停止;
(2)吸收反应生成的二氧化硫;
(3)防止炸裂集气瓶
点评 本题主要考查仪器的用途、反应表达式的书写,实验装置的选择,选择发生装置时,要考虑反应物的状态、反应条件等因素;选择收集装置时,要考虑气体的水溶性、能否和水发生化学反应、密度、能否和空气中的物质发生化学反应等因素.


科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
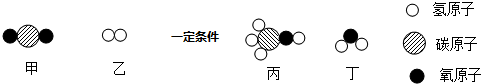
| A. | 该反应是置换反应 | |
| B. | 反应前后分子总数不变 | |
| C. | 发生反应的甲和乙的质量比为22:3 | |
| D. | 反应前后各元素的化合价不发生变化 |
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | IrO4+ | B. | IrO5+ | C. | IrO3+ | D. | IrO2+ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com