

分析 【实验设计】
(1)根据酸能与碱发生中和反应分析回答;
(2)根据一氧化碳与空气的混合气体点燃时易发生爆炸分析回答;
(3)根据浓硫酸具有吸水性、一氧化碳与氧化铜的反应、二氧化碳与氢氧化钙的反应分析回答;
(4)根据题干中的反应,写出反应的化学方程式;
【反思与评价】一氧化碳有毒,能污染空气.
解答 解:【实验设计】
(1)草酸是一种酸,能与碱发生中和反应.
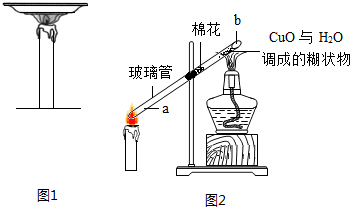
(2)由于一氧化碳与空气的混合气体点燃时易发生爆炸,该兴趣小组进行上述实验时,从实验安全的角度考虑,该先点燃A处的酒精灯,产生的一氧化碳将玻璃管内的空气排干净后再点燃B处的酒精灯;
(3)浓硫酸具有吸水性,D装置的作用是干燥气体;若通过F装置中澄清石灰水变浑浊来证明草酸亚铁晶体受热分解的气体产物中有CO,则需在C和D装置之间增加盛有澄清石灰水的洗气瓶H.现象为黑色的氧化铜逐渐变成红色,F装置中澄清石灰水变浑浊时可证明产物中有CO.
(4)若B中无水硫酸铜变蓝说明了有水生成;C中装置质量增大,说明有二氧化碳生成;E中黑色粉末变红,F中澄清石灰水变浑浊,说明了由二氧化碳生成.则装置F中发生反应的化学方程式:CO2+Ca(OH)2═CaCO3↓+H2O.草酸亚铁晶体受热分解的化学方程式:FeC2O4•2H2O$\frac{\underline{\;\;△\;\;}}{\;}$FeO+CO↑+CO2↑+2H2O↑;
【反思与评价】从环保角度考虑,该套实验装置的明显缺陷是没有尾气处理装置,这时因为CO 有毒,排放到空气中会造成空气污染.
故答为:【实验设计】
(1)草酸能与碱发生中和反应;(2)A;(3)干燥气体;黑色的氧化铜逐渐变成红色,F装置中澄清石灰水变浑浊;(4)CO2+Ca(OH)2═CaCO3↓+H2O,FeC2O4•2H2O$\frac{\underline{\;\;△\;\;}}{\;}$FeO+CO↑+CO2↑+2H2O↑;
【反思与评价】有毒.
点评 化学实验现象是化学实验最突出、最鲜明的部分,也是进行分析推理得出结论的依据,掌握物质的性质和相互之间的反应关系,并有助于提高观察、实验能力.所以,对化学实验不仅要认真观察,还应掌握观察实验现象的方法.


 数学奥赛暑假天天练南京大学出版社系列答案
数学奥赛暑假天天练南京大学出版社系列答案科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
| 反应前物质的质量/g | 反应后物质的质量/g | |
| Cu-Zn合金 | 稀硫酸 | 滤液 |
| 4.0 | 10 | 11.26 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
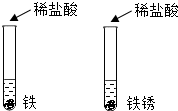 为了探究盐酸除铁锈的实验中,气体是由什么产生的,设计如下实验:(1)在两支试管分别放入铁粉和铁锈;(2)分别加入等量等浓度的稀盐酸,观察现象.针对该实验的目的,下列评价或改进正确的是( )
为了探究盐酸除铁锈的实验中,气体是由什么产生的,设计如下实验:(1)在两支试管分别放入铁粉和铁锈;(2)分别加入等量等浓度的稀盐酸,观察现象.针对该实验的目的,下列评价或改进正确的是( )| A. | 该实验步骤正确完整 | |
| B. | 应补充一个铁与水反应的实验 | |
| C. | 应补充一个铁锈与水反应的实验 | |
| D. | 应补充一个铁锈与水反应的实验和补充一个铁与水反应的实验 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
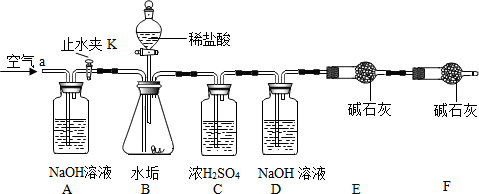
| 阴离子 阳离子 | OH- | CO32- | HCO3- |
| Ca2+ | 微溶 | 不溶 | 可溶 |
| Mg2+ | 不溶 | 微溶 | 可溶 |
| 实验步骤 | 实验现象 | 结论 |
| 在少量研碎的水垢中,加入适量的蒸馏水充分搅拌,过滤,在滤液里加入Na2CO3溶液. | 无白色沉淀 | 水垢中无Ca(OH)2 |
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com