
科目:初中化学 来源: 题型:选择题
| A. | 氢氧化钠固体易潮解,有腐蚀性,称量时不能直接放在天平的托盘上 | |
| B. | 氧气可以支持燃烧,具有可燃性 | |
| C. | 经常用钢丝球洗刷铝锅,能使之光亮、耐用 | |
| D. | 钢铁闸门浸入水下的部分比靠近水面的部分更容易生锈 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | ①只能表示氢元素 | |
| B. | ③只能表示铜原子 | |
| C. | ③④⑤能表示物质的化学式 | |
| D. | ②中的“2”表示铁离子带2个单位正电荷 |
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
| 实验方案 | 预期现象 | 结论 |
| 步骤1:取一定量的合金粉末,加过量的氢氧化钠溶液 | 固体部分溶解,有气泡产生 | 合金中一定含有铝 |
| 步骤2:取少量合金粉末,加过量的稀盐酸 | 固体部分溶解,有气泡产生,溶液由无色变为浅绿色 | 假设4成立 |
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
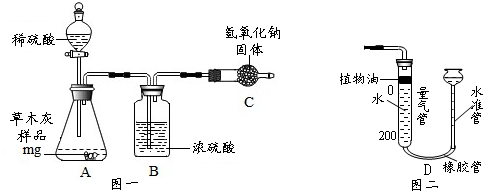
| 实验序号 | 实验操作 | 实验现象 | 实验结论 |
| 实验一 | 取样,加入足量的稀盐酸,将生成的气体通入澄清的石灰水 | 石灰水变浑浊 | 该晶体中含有碳酸根离子 |
| 实验二 | 取样,溶于水滴入酚酞 | 溶液变红色 | 溶液呈碱性 |
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
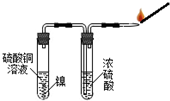 某研究性学习小组的同学为探究金属镍(Ni,银白色金属)和铜的活动性顺序,进行了一系列实验活动.请你一起参与他们的活动,并回答有关问题.
某研究性学习小组的同学为探究金属镍(Ni,银白色金属)和铜的活动性顺序,进行了一系列实验活动.请你一起参与他们的活动,并回答有关问题.| 实验方案 | 实验现象 | 实验结论 |
| 将金属镍加入到盛有硫酸铜溶液的试管中 | 溶液的颜色变浅, 有红色固体析出 | 镍比铜的金属活动性强 |
查看答案和解析>>
科目:初中化学 来源: 题型:填空题

查看答案和解析>>
科目:初中化学 来源: 题型:解答题
| 物 质 | 所需时间 | 价 格 |
| 铁屑 | 约13900s | 10.00元/1000g |
| 锌粒 | 约50s | 20.00元/500g |
| 镁片 | 约20s | 10.80元/25g |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com