
【题目】实验研究是化学学习的重要方法。请以碳及其化合物的知识进行以下实验研究。
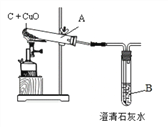
实验一:木炭还原氧化铜。
①观察到B中溶液变浑浊,试管A中的现象_______________,
A中反应的化学方程式为________,还原剂是__________。
②反应完全后,若先撤走酒精喷灯停止加热,可能导致的后果___________________________
实验二:为了探究某混合气体是由水蒸气、一氧化碳、二氧化碳3种气体组成, 设计了如下实验:
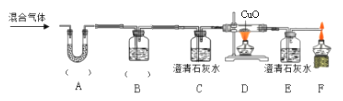
①欲探究混合气体中含有CO2和H2O蒸气,在图中的A、B装置内依次盛放的化学试剂为_______;检验出水蒸气的现象是_____________,反应的化学方程式为__________。
②装置E、F的作用分别是__________________ 、_____________________,E中反应的化学方程式为_____________。
③若没有装置E_______________(填“能”或“否”)证明混合气体中含有一氧化碳,请简述理由_____________________。
④实验结束后先熄灭装置D处的酒精灯,E中石灰水不会倒流的原因是____________。
⑤该实验中体现的一氧化碳的化学性质有__________________________。
实验三:有些化妆品中添加的高纯度碳酸钙可以用石灰石来制备,如下图。(假设石灰石中除碳酸钙外。所含杂质仅为SiO2,其不溶于水,高温不会分解,也不与盐酸反应)
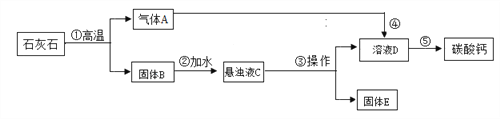
Ⅰ. 写出步骤①②中反应的化学方程式____________、____________。
Ⅱ. 气体A能使紫色石蕊试液变红色,反应的化学方程式为____________ 。
Ⅲ. 操作⑤的目的是________,用到的仪器主要有玻璃棒、酒精灯、铁架台(带铁圈)、__________。
Ⅳ. 为验证实验结束后得到的固体B中碳酸钙是否已经完全分解,请设计两种方案完成下表内容。
实验步骤 | 实验现象 | 结论 | |
方案一(66) | ________________ | ________________ | ________________ |
方案二(67) | ________________ | ________________ | ________________ |
【答案】 黑色固体变成亮红色 ![]() C或碳 石灰水流入热的试管,热的试管炸裂 无水硫酸铜 无水硫酸铜由白色粉末变成蓝色晶体
C或碳 石灰水流入热的试管,热的试管炸裂 无水硫酸铜 无水硫酸铜由白色粉末变成蓝色晶体 ![]() 检验一氧化碳与氧化铜反应是否产生了CO2 点燃尾气,防止污染空气
检验一氧化碳与氧化铜反应是否产生了CO2 点燃尾气,防止污染空气 ![]() 能 因为混合气体中没有其它还原性气体,氧化铜由黑色变成亮红色,说明有CO(合理给分) 因为熄灭酒精灯后,会继续通入气体,直到装置D的玻璃管冷却。 还原性、可燃性
能 因为混合气体中没有其它还原性气体,氧化铜由黑色变成亮红色,说明有CO(合理给分) 因为熄灭酒精灯后,会继续通入气体,直到装置D的玻璃管冷却。 还原性、可燃性 ![]()
![]() CO2 + H2O= H2CO3 过滤(或过滤、洗涤、烘干) 漏斗(或漏斗、烧杯) 用一支洁净试管取适量固体B,滴加足量稀盐酸 有气泡产生 碳酸钙部分分解 取适量固体B放入一支洁净硬质试管,高温加热,将产生气体通入澄清石灰水 澄清石灰水变浑浊 碳酸钙部分分解
CO2 + H2O= H2CO3 过滤(或过滤、洗涤、烘干) 漏斗(或漏斗、烧杯) 用一支洁净试管取适量固体B,滴加足量稀盐酸 有气泡产生 碳酸钙部分分解 取适量固体B放入一支洁净硬质试管,高温加热,将产生气体通入澄清石灰水 澄清石灰水变浑浊 碳酸钙部分分解
【解析】实验一:①木炭和氧化铜在高温的条件下生成同和二氧化碳,故观察到B中溶液变浑浊,试管A中的现象是:黑色固体变成亮红色,A中反应的化学方程式为![]() ,还原剂是碳;②反应完全后,若先撤走酒精喷灯停止加热,可能导致的后果是:石灰水流入热的试管,热的试管炸裂;实验二:①欲探究混合气体中含有CO2和H2O蒸气,由于澄清石灰水中含有水,所以应先探究水,后探究二氧化碳,所以在图中的A、B装置内依次盛放的化学试剂为无水硫酸铜、澄清石灰水;检验出水蒸气的现象是无水硫酸铜由白色粉末变成蓝色晶体,反应的化学方程式为
,还原剂是碳;②反应完全后,若先撤走酒精喷灯停止加热,可能导致的后果是:石灰水流入热的试管,热的试管炸裂;实验二:①欲探究混合气体中含有CO2和H2O蒸气,由于澄清石灰水中含有水,所以应先探究水,后探究二氧化碳,所以在图中的A、B装置内依次盛放的化学试剂为无水硫酸铜、澄清石灰水;检验出水蒸气的现象是无水硫酸铜由白色粉末变成蓝色晶体,反应的化学方程式为![]() ;②装置E、F的作用分别是检验一氧化碳与氧化铜反应是否产生了CO2 、点燃尾气,防止污染空气,E中反应的化学方程式为
;②装置E、F的作用分别是检验一氧化碳与氧化铜反应是否产生了CO2 、点燃尾气,防止污染空气,E中反应的化学方程式为![]() ;③若没有装置E也能证明混合气体中含有一氧化碳,因为混合气体中没有其它还原性气体,氧化铜由黑色变成亮红色,说明有CO;④实验结束后先熄灭装置D处的酒精灯,E中石灰水不会倒流的原因是:熄灭酒精灯后,会继续通入气体,直到装置D的玻璃管冷却;⑤该实验中体现的一氧化碳的化学性质有一氧化碳还原氧化铜体现出还原性,一氧化碳能燃烧,体现出可燃性;实验三:Ⅰ. 写出步骤①②中反应的化学方程式分别为:
;③若没有装置E也能证明混合气体中含有一氧化碳,因为混合气体中没有其它还原性气体,氧化铜由黑色变成亮红色,说明有CO;④实验结束后先熄灭装置D处的酒精灯,E中石灰水不会倒流的原因是:熄灭酒精灯后,会继续通入气体,直到装置D的玻璃管冷却;⑤该实验中体现的一氧化碳的化学性质有一氧化碳还原氧化铜体现出还原性,一氧化碳能燃烧,体现出可燃性;实验三:Ⅰ. 写出步骤①②中反应的化学方程式分别为: ![]() ;
; ![]() ;Ⅱ. 二氧化碳与水反应生成碳酸,碳酸能使紫色石蕊试液变红色,反应的化学方程式为:CO2 + H2O
;Ⅱ. 二氧化碳与水反应生成碳酸,碳酸能使紫色石蕊试液变红色,反应的化学方程式为:CO2 + H2O![]() H2CO3;Ⅲ. 操作⑤的目的是过滤,使固液分离,用到的仪器主要有玻璃棒、酒精灯、铁架台(带铁圈)、漏斗、烧杯;Ⅳ. 为验证实验结束后得到的固体B中碳酸钙是否已经完全分解,设计两种方案如下:
H2CO3;Ⅲ. 操作⑤的目的是过滤,使固液分离,用到的仪器主要有玻璃棒、酒精灯、铁架台(带铁圈)、漏斗、烧杯;Ⅳ. 为验证实验结束后得到的固体B中碳酸钙是否已经完全分解,设计两种方案如下:
实验步骤 | 实验现象 | 结论 | |
方案一(66) | ____用一支洁净试管取适量固体B,滴加足量稀盐酸____________ | ___有气泡产生_____ | ___碳酸钙部分分解____ |
方案二(67) | __取适量固体B放入一支洁净硬质试管,高温加热,将产生气体通入澄清石灰水__ | ___澄清石灰水变浑浊___ | __碳酸钙部分分解 ___ |


 阅读快车系列答案
阅读快车系列答案科目:初中化学 来源: 题型:
【题目】用木炭还原氧化铜的实验如图.
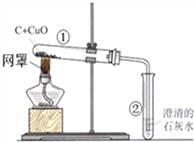
(1)酒精灯加灯罩的目的 ______ ;
(2)加热一段时间后,可观察到的现象________________、_________________________
(3)请你写出①②试管中发生反应的化学方程式:
① _________________________________ ② ________________________
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】实验室里既可用高锰酸钾(或氯酸钾和二氧化锰的混合物)在加热条件下使其分解制取氧气,也可用如图装置,通过分解过氧化氢(H2O2)来制取氧气。
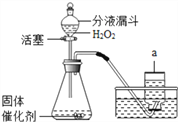
请你根据已学化学知识和经验回答下列问题:
(1)写出过氧化氢分解制氧气的化学方程式:_______________。
(2)写出如图装置中仪器a的名称:__________ 。
(3)与高锰酸钾(或氯酸钾和二氧化锰的混合物)制取氧气相比,用过氧化氢制取氧气的优点是:__________________。
(4)收集氧气的方法还可用_______________法,你选择此方法的理由是:_____________。
(5)如用如图所给的发生装置还可以制取的气体有_________________。
(6)如图发生装置中用分液漏斗而不用长颈漏斗的优点是:_______________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】已知氯化钠、碳酸钠在不同温度时的溶解度如下:
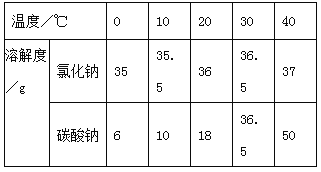
⑴依据上表数据,绘制出了氯化钠和碳酸钠的溶解度曲线(如下图),图中能表示碳酸钠
溶解度曲线的是________(填“A”或“B”)。
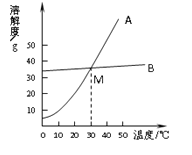
⑵图中两溶解度曲线相交于M点,此点表示的意义是____________________________。
⑶40℃时,把50 g A物质放入100 g水中,充分搅拌,所得溶液是________________溶液(填“饱和”或“不饱和”)。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】利用数字化实验可以形象地比较不同形状的碳酸钙与稀盐酸反应的速率。倾斜锥形瓶使试管内的稀盐酸流入瓶中与固体发生反应,瓶内气压的变化如曲线所示。
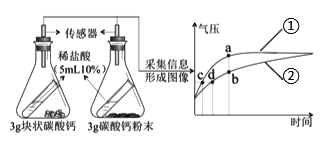
有关说法正确的是
A. 曲线①表示块状碳酸钙与稀盐酸反应
B. b点表示碳酸钙与盐酸反应已停止
C. 等质量的碳酸钙,粉末状的产生CO2的质量多
D. 对比分析点c、d可知,相同的气压时,粉状碳酸钙与稀盐酸反应速率更快
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】逻辑推理是化学学习常用的思维方法,下列推理不正确的是( )
A. 碱的溶液呈碱性,呈碱性的溶液不一定是碱溶液
B. 置换反应一定有单质生成,有单质生成的反应不一定是置换反应
C. 氧化物中一定含氧元素,含氧元素的化合物一定是氧化物
D. 单质中只含有一种元素,则只含有一种元素的纯净物一定是单质
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】化学为人类社会的可持续发展做出了巨大贡献目前人类使用的主要能源是化石燃料,会加剧温室效应。发展“低碳生活”是当今社会发展的趋势。
(1)化石燃料指的是_______、_______、_______。
(2)下列做法符合“低碳生活”的是_______。
①提倡使用一次性筷子 ②步行代替开私家车 ③日常生活耗用的能量尽量少
(3)舍勒是最早制得氧气的化学家之一,他获得氧气的方法主要有以下两种:
a.加热分解硝酸钾、氧化汞、硝酸银等
b.用二氧化锰与浓硫酸加热:![]()
①a中反应物均可制得氧气,因为他们组成的共同点是______
②b中物质X的化学式是______,H2SO4的一个分子中有______个原子。
(4)拉瓦锡通过定量分析实验,获得化学的重要定律——质量守恒定律。
①由质量守恒定律可知,化学反应前后一定不变的是______(填字母序号,下同),可能变化的是______。
A.原子种类 b.原子数目 c.分子种类 d.分子数目 e.元素种类 f.物质种类
②已知5gX恰好与10gY化合生成新物质Z。现有X、Y各15g,完全反应后生成Z的质量为______g。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】有一份锌粉与铜粉的混合物样品,为确定其组成,某同学将32.5 g样品加入100 g稀硫酸中,恰好完全反应,放出气体的质量与反应时间的关系如下图所示。试求:

(1)样品中金属铜的质量是 g。
(2)所用稀硫酸的溶质质量分数(写出计算过程)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com