
����Ŀ��ij���Na2CO3����Ʒֻ�����������Ȼ������ʣ��ֳ�ȡ6g���������ձ��в�����ϡ���ᣬ��ϡ����μ���36.5gʱ���ձ�����Һ��������Ϊ40.3g������������ȫ���ݳ������ҵõ���������Һ����������������������ϡ�����������ϵ��ͼ��ʾ���Լ��㣺
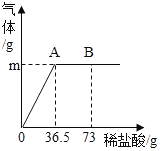
��1��m��ֵ��_____��
��2��B��ʱ���ձ�����Һ�����ʵĻ�ѧʽ_____��
��3���պ���ȫ��Ӧʱ��������Һ��������������____�������м�����̣������ȷ��0.1%����
���𰸡�2.2g NaCl��HCl 16.3%
��������
�⣺��1����ͼ���Կ�������������ﵽ36.5g��ʱ������ﵽ���������ǡ����ȫ��Ӧ�����������غ㶨�ɿɵã����ɵĶ�����̼������Ϊ6g+36.5g��40.3g��2.2g��
��2����B��ʱ�������Ѿ����������Դ�ʱ����Ϊ���ɵ��Ȼ��ƺ�ʣ������ᣬ�仯ѧʽ�ֱ�Ϊ��NaCl��HCl��
��3����μӷ�Ӧ��̼���Ƶ�����Ϊx�����ɵ��Ȼ��Ƶ�����Ϊy
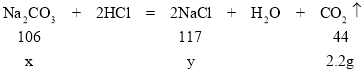
106��44=x��2.2g x��5.3g
117��44=y��2.2g y��5.85g
�պ���ȫ��Ӧʱ��������Һ��������������Ϊ![]() ��100%��16.3%
��100%��16.3%
�𣺣�1��m��ֵ��2.2g��
��2��B��ʱ���ձ�����Һ�����ʵĻ�ѧʽ NaCl��HCl��
��3���պ���ȫ��Ӧʱ��������Һ��������������Ϊ16.3%



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����֪�����ͺ��Ļ�ѧ�������ơ�ͬѧ������ͼװ�òⶨ�����������ĺ�����
![]()
������ͼ��ʾ���ڲ������з����������ף�����ע�����Ͳ�������ɵ��ܱ�ϵͳ�ڹ���60 mL����������װ�а��IJ�����������ȼ��
�ڽ����ƶ�����ע�����Ļ�����ȼ�ŵİ���Ϩ��
�۵�ע�������������ƶ�ʱ����ȡע��������������
�����������з�����ѧ��Ӧ�ķ��ű���ʽΪ______��
��������ڵ�Ŀ����______��
����������У���ע�������������ƶ�ʱ���ܱ�ϵͳ���������Ϊ______mL��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����Һ�����ǵ�����ϢϢ��ء�
��1����ʢ��ˮ���ձ��м�������ij�����ʣ��γ���Һ�����У��¶����ߡ�����������_____������ĸ����
A�ռ� B����� C�Ȼ���
��2�����ұ����й������ʵ��ܽ����������ͼ��ʾ���ش��������⡣

��t1��ʱ���ס��ҡ��������ʵ��ܽ���ɴ�С��˳����_____��
��t2��ʱ�����ҵ��ܽ��_____�����ȡ�����ȡ�����
��t2��ʱ�������ʵı�����Һ���������ܼ���������Ϊ_____����д���ȣ�
��t3�潫�Һͱ��������ʵı�����Һ���͵�t1�棬������Һ�����ʵ�����������С��ϵΪ��_____�������������������=������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ij��ѧ��ȤС��������ͼһ��ͼ��������װ��̽����ȡ�����ԭ�������������ʡ����ͼ���ش��������⣺��װ�������Զ��Ѽ����ϣ�
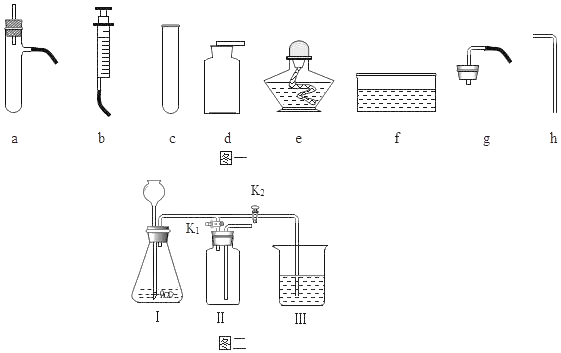
��1��д��ͼһ�����������ƣ�e_____��f_____��
��2���ѹ���������Һ��������ʢ�ж������̵���������ȡ���ռ���������ɸ�ʵ������ѡ�õ�������_____����ĸ����д���÷�Ӧ�Ļ�ѧ����ʽ_____��
��3�����ַ��������Ѷ������̼���ʢ�й���������Һ���Թ����������������_____���ŵ㡣��д��һ�����ɣ�
��4����С�����������ͼ����ʾ��ʵ��װ�ã��ȿ�������ȡ���壬�ֿ�����̽���������ʡ�
�ٵ���K1���ر�K2ʱ������I����װ�ã��ɽ��е�ʵ����_____������ĸ����
a ����ʯ��ϡ���ᷴӦ��ȡ������̼
b п��ϡ���ᷴӦ��ȡ����
�ڵ���K2���ر�K1ʱ����������ͼװ���Ƶö�����̼����֤�����ʡ���Ҫ֤��������̼����ˮ������Ӧ��Ӧ���ձ����ˮ�м���_____�����з�����Ӧ�Ļ�ѧ����ʽΪ_____��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���û�ѧ���Ԫ�ط��š����ӷ��š���ѧʽ����ѧ����ʽ����գ�
��1��������������_____��
��2��̼��+2 ��������_____��
��3���ɿ����к�������Ԫ�ء��ؿ��к������ķǽ���Ԫ�غ͵ؿ��к������Ľ��� Ԫ�ع�ͬ��ɵĻ�����Ļ�ѧʽ_____��
��4���ڳ����Ĵ������£����������������Ӧ������������SO3����_____��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��±ˮ����Ҫ�ɷּ����ܽ��������ͼ��ʾ��
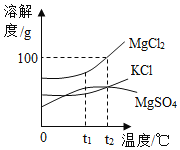
��1��t1��ʱ��MgSO4���ܽ��_______����������������������=����KCl���ܽ�ȡ�
��2����t1��ʱ��MgCl2��KC1��MgSO4�������ʵı�����Һ�ֱ�������t2��ʱ���о�����������_______��
��3��t2��ʱ��50gˮ������ܽ�MgCl2������Ϊ_______g��
��4����ʹMgCl2�ı�����Һ��Ϊ��������Һ�����Բ�ȡ�Ĵ�ʩ��_______������һ�֣���
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����㸡�����dz��õĻ�ѧ����������Ҫ�ɷ��ǹ���̼���ƣ�2Na2CO33H2O2��������ˮ��Ѹ������ˮ����������������缰��������ɻ��ʡ�ij��ѧ��ȤС������㸡�����Ļ�ѧ���ʡ�����ԭ��������̽����
���������ϣ�a.����̼���ƾ���̼���ƺ��������˫�����ʣ���ˮ��Һ�к���Na+��OH-��CO32-��H2O2��
b.Na+���ܴ���������ֽ⡣
c.��ͬ�¶��£�pH��ͬ����Һ��OH-��Ũ��Ҳ��ͬ��
̽��һ����̼���ƵĻ�ѧ����
ʵ�鲽�� | ʵ������ | ʵ����ͣ���ѧ����ʽ�� |
1��ȡ��������ˮ���μ�_______��Һ | �а�ɫ�������� | / |
2��ȡ��������ˮ������������̷�ĩ | _______ | _______ |
̽�������㸡��������ԭ��
��������⣩����̼������Һ�е��������Թ�������ֽ��д����ã�
��������裩����һ��CO32- �������OH-��������______________
��ʵ����̣���ͬ�¶��£�����H2O2��Һ�Լ�H2O2��Һ�зֱ��Na2CO3��NaOH��ʵ�飬�ⶨ��ͬʱ������Һ��pH���ܽ���������mg/L�����������£�
ʵ����� | 1 | 2 | 3 | 4 |
�Լ� | H2O2 | H2O2+Na2CO3 | H2O2+NaOH | H2O2+NaOH |
pH | 6.01 | 8.14 | 8.14 | 9.26 |
�ܽ��� | 6.44 | 9.11 | 9.11 | 10.97 |
��ʵ����ۣ��Ա�ʵ�����ݣ�֤������_______��ȷ��
����˼���������ʵ��2��3��Ŀ����_______��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���������ڼ䣬�������ͣ���˴������洬����ش��������⣺
��1�������洬���淢����ʴ��������Ϊ_____��
��2��������ϴ�Ӽ���ϴ�������ۣ���������ϴ�Ӽ���_____���ܡ����Ԫ����ɵĽǶ�˵����ˮ����͡������ܵ�ԭ����_____��
��3���洬�ϵ�ľ��Ʒ��Ϊȼ���ṩ��_____����ȼ�յ�����֮һ�����洬��Я���иɷ���������ɷ���Ҫ�ɷ���NaHCO3�����Ⱥ�������Na2CO3��CO2��һ���������д�÷�Ӧ�Ļ�ѧ����ʽ_____��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��A~F��Ϊ���л�ѧ���������ʣ�����֮��Ĺ�ϵ����ͼ��ʾ(��������ʾת����ϵ���漰��ӦΪ���г�����Ӧ)������ A ����Ϊ��ʯ�ң�CΪ�������ܼ���C �� E Ԫ�������ͬ����ش���������:
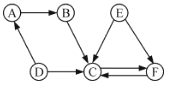
(1)F �Ļ�ѧʽΪ______��
(2)B ��ũҵ�ϵ���;��______(дһ��)��
(3)ת����û���漰�Ļ�����Ӧ������______ ��
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com