

| 实验操作 | 实验现象 | 实验结论 |
| (1)取少量固体放于试管中,加足量蒸馏水溶解,静置后取上层清液滴加无色酚酞溶液 | 固体溶解时试管外壁发烫,试管底部有不溶物,溶液变红. | 固体中一定含有 和氢氧化钙. |
| (2)另取少量固体放于试管中,滴加足量的 |
固体逐渐消失,有大量无色气体产生,得到浅绿色溶液. | 固体中一定含有 一定不含Fe2O3 |

| 实验操作 | 实验现象 | 实验结论 |
| 取少量固体于试管中,滴加足量的稀盐酸,并将气体通入澄清石灰水 | 固体逐渐消失、有气泡冒出、溶液变为黄色、澄清的石灰水变浑浊 | 固体中一定含有 |
| 74 |
| 100 |
| x |
| 1.0g |
| 56 |
| 74 |
| 0.6g |
| y |


科目:初中化学 来源: 题型:
| A、氢氧化钙-熟石灰 碱 |
| B、氢氧化钠-纯碱 碱 |
| C、碳酸氢钠-苏打 盐 |
| D、氧化钙-消石灰 氧化物 |
查看答案和解析>>
科目:初中化学 来源: 题型:
| 序号 | H2O2溶液的浓度 | 30% | 15% | 10% | 5% |
| 1 | 无催化剂、不加热 | 几乎不反应 | 几乎不反应 | 几乎不反应 | 几乎不反应 |
| 2 | 无催化剂、加热 | 360 | 480 | 540 | 720 |
| 3 | MnO2催化剂、加热 | 10 | 25 | 60 | 120 |
查看答案和解析>>
科目:初中化学 来源: 题型:
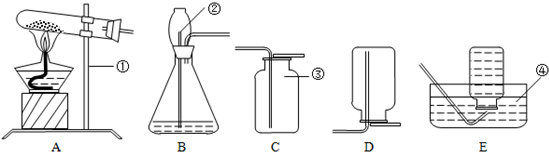
查看答案和解析>>
科目:初中化学 来源: 题型:
查看答案和解析>>
科目:初中化学 来源: 题型:
| 水质主要成分 (mg/L) Ca2+50.2~75.3 Mg2+17.8~26.2 K+0.62~3.25 Na+ 18.7~29.8 HCO3- 184~261 Cl-14.2~30.8 SO42-41.6~70.2 |
 原子结构示意图判断,该元素原子的核电荷数为
原子结构示意图判断,该元素原子的核电荷数为| 化学符号 | Ca2+ | Mg2+ | HCO3- | SO42- |
| 化合价 | +2 | +2 | -1 | -2 |
查看答案和解析>>
科目:初中化学 来源: 题型:

查看答案和解析>>
科目:初中化学 来源: 题型:
 某化学小组在学习酸、碱化学性质时,做了如下实验 (如图),将等质量的稀盐酸和氢氧化钙溶液混合后得到一种无色溶液.
某化学小组在学习酸、碱化学性质时,做了如下实验 (如图),将等质量的稀盐酸和氢氧化钙溶液混合后得到一种无色溶液.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com