
【题目】A-E均是初中化学中常见的化合物,它们之间存在如图转化关系.其中B是一种常见的氧化物,且可与D在常温下发生反应。A,B,E含有相同的元素,A,C,D也含有相同的元素。请回答下列问题 (注:部分反应物或生成物已略去)
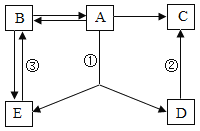
(1)B的化学式为_________, A的俗称_________。
(2)写出图中反应①的化学方程式____________________________________
【答案】CO2 苏打或纯碱 ![]()
【解析】
B是一种常见的氧化物,且可与D在常温下发生反应,初中常见能在常温下反应的氧化物有H2O和CO2,且B与A和E都可相互转化,只能是CO2与碳酸盐的相互转化,故B为CO2,A、E都为碳酸盐,且A可生成E,由复分解反应规律可知E一定为沉淀,常见的碳酸盐沉淀为CaCO3,故E为CaCO3,A可能为Na2CO3,则D可能为NaOH,因为A,C,D也含有相同的元素,故由图像关系可推出C为NaCl。
(1)B的化学式为CO2,A为Na2CO3其俗称为苏打或纯碱;
(2)反应①为Na2CO3反应生成CaCO3和NaOH,根据复分解反应规律可知其反应方程式为![]() 。
。


 阅读快车系列答案
阅读快车系列答案科目:初中化学 来源: 题型:
【题目】实验室制取气体所需装置如下图所示.
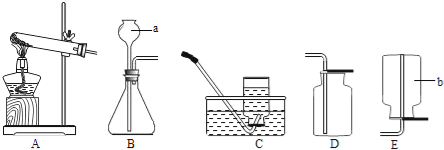
(1)实验仪器a、b的名称是a 、b .
(2)用大理石和稀盐酸制取二氧化碳时,所选用的发生装置是 (填序号),其反应的化学方程式是 .
(3)用高锰酸钾制取氧气,其反应的化学方程式是 .将装置A和C连接进行此实验,实验结束,停止加热前要先将导管移出水面,目的是 .
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】将锌加入到一定质量的AgNO3和Cu(NO3)2的混合溶液中,溶液的质量与加入Zn的质量关系如下图所示,下列说法正确的是( )
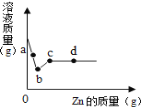
A.a至b段(不包含b点)所含溶质有2种
B.b点得到的固体为Cu
C.c点比a点所含溶质种类少
D.d点得到的固体有2种
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】在一个密闭容器中放入X、Y、Z、W四种物质,在一定条件下发生化学反应,一段时间后,测得有关数据如下表:
物 质 | X | Y | Z | W |
反应前的质量(g) | 20 | m | 16 | 14 |
反应后的质量(g) | 4 | 6 | 60 | 50 |
下列关于此反应的认识,正确的是( )
A.m的数值为64
B.Z和W的相对分子质量之比为11:9
C.参加反应的X与Y的质量比为1:4
D.若X为化合物,Y为单质,则该反应一定为置换反应
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】向一定质量的Na2CO3、Na2SO4混合溶液中先后滴加BaCl2、HCl溶液,反应过程中加入溶液的质量与产生沉淀或气体的质量关系如图所示,下列说法正确到是( )
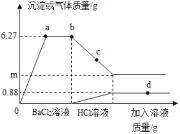
A. 0﹣a段发生了一个反应
B. c点沉淀的成分为一种
C. 取d点对应的溶液,滴加硝酸银溶液,有白色沉淀,说明加入的盐酸已过量
D. m=2.33
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】某溶液由盐酸、稀硫酸、氢氧化钾、氯化镁中的一种或几种混合而成。现向该混合溶液中滴入氢氧化钡溶液,产生沉淀质量与加入氢氧化钡溶液体积如图所示。则
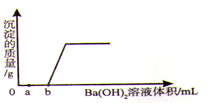
(1)该溶液中一定没有的溶质是 。
(2)a点对应的溶液中一定含有的溶质是 。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】为了测定某硫酸钠和氯化钠样品中硫酸钠的纯度,取200g样品,分别在5只烧杯中进行实验,实验数据如下(杂质不溶于水,也不和稀盐酸反应)
烧杯1 | 烧杯2 | 烧杯3 | 烧杯4 | 烧杯5 | |
加入样品的质量g | 40 | 40 | 40 | 40 | 40 |
加入氯化钡溶液的质量g | 50 | 100 | 150 | 200 | 250 |
充分反应后生成沉淀的质量g | 11.65 | 23.3 | 34.95 | 46.6 | 46.6 |
(1)烧杯________(填序号)中的物质恰好完全反应。
(2)求样品中硫酸钠的纯度_________。
(3)求恰好完全反应时所得溶液的溶质质量分数__________。(计算结果精确至0.1%)
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】请回答下列问题.
(1)工业上从含有金属元素并有开采价值的矿石提炼金属,以下金属矿石中可用于冶炼铝的是___(填序号).

(2)金属材料包括纯金属以及它们的___.铁制品锈蚀的主要条件是铁与___和___同时接触.
(3)将m克Zn和Mg的混合物中加入一定质量的CuCl2溶液,充分反应后过滤,将滤渣洗涤、干燥后称量。质量仍为m克,对所得滤液和滤渣有如下四种判断:
A 滤液可能是无色
B 滤液中一定有ZnCl2和MgCl2
C 滤渣中的物质可能有3种
D 滤渣中加稀盐酸一定有气泡产生
以上判断正确的是____(填序号)。
(4)现有两瓶失去标签的溶液,溶质分别可能是氯化钠、硝酸铜、硫酸钠、硝酸、硫酸、碳酸钠中的一种,检验步骤如下:
Ⅰ.分别取少量混合,无明显现象,溶液无色透明,经测定混合溶液显酸性。由此可推断这两瓶溶液中的溶质一定不是____;(填化学式,多填、少填、错填均不得分,下同)
Ⅱ.向上述混合溶液中加入Ba(NO3)2溶液,产生白色沉淀。则这两瓶溶液中的溶质至少是____中的一种;试推断这两瓶溶液的溶质可能的组合有_____种(填数字)。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】某化学兴趣小组进行草酸亚铁晶体(FeC2O42H2O)分解的实验探究。
【猜 想】草酸亚铁晶体分解会产生CO、CO2和H2O三种气体。
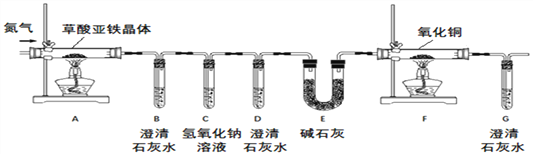
【实验方案】按照上图装置进行实验(夹持装置未画出)。
【问题讨论】(1)实验开始前需要先鼓入一段时间的N2,该操作的目的为_________;
(2)C中氢氧化钠溶液的作用是_______;
(3)E中碱石灰的作用是___________;
【结果分析】(4)定性分析:
①试管D中出现浑浊,证明产物中有_____存在;证明分解产物中存在CO的现象是_____。
②小明认为应增加H装置,则H装置应放在____两个装置之间,若观察到____,则证明有水生成;
(5)定量分析(假定每一步反应进行完全):取3.6g样品进行上述实验,测得装置A硬质玻璃管中残余1.44g黑色固体FeO,装置F中硬质玻璃管固体质量减轻0.32g,则草酸亚铁晶体(FeC2O42H2O)分解得到的CO2的质量为______。
【反思评价】(6)从环保角度考虑,该套实验装置的明显缺陷是______;
(7)文献显示,FeC2O42H2O受热分解时,固体的质量随温度变化的曲线如下图所示,写出加热到400oC时,FeC2O42H2O受热分解的化学方程式_______。
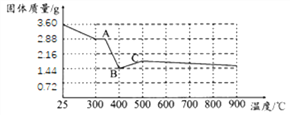
根据图像,若有3.6gFeC2O42H2O在敞口环境中充分加热,最终得到红棕色固体1.60g,则该物质的化学式为_______。由此,你认为进行该实验需要注意的事项是________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com