
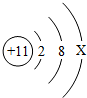 ,其中X=1,该原子在化学反应中易失电子,形成的粒子名称为钠离子,该粒子与氧离子构成的化合物的化学式为Na2O.
,其中X=1,该原子在化学反应中易失电子,形成的粒子名称为钠离子,该粒子与氧离子构成的化合物的化学式为Na2O.  教学练新同步练习系列答案
教学练新同步练习系列答案 课前课后同步练习系列答案
课前课后同步练习系列答案 课堂小作业系列答案
课堂小作业系列答案 黄冈小状元口算速算练习册系列答案
黄冈小状元口算速算练习册系列答案 成功训练计划系列答案
成功训练计划系列答案 倍速训练法直通中考考点系列答案
倍速训练法直通中考考点系列答案科目:初中化学 来源: 题型:填空题
 眼镜是人们常用的护眼工具.如图是一款变色眼镜的示意图:
眼镜是人们常用的护眼工具.如图是一款变色眼镜的示意图:查看答案和解析>>
科目:初中化学 来源: 题型:解答题


查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 用熟石灰改良碱性土壤 | |
| B. | pH<5.6的雨水称为酸雨 | |
| C. | “温室效应”主要是由CO2等气体引起的 | |
| D. | 使用乙醇汽油能减少污染,节约石油资源 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
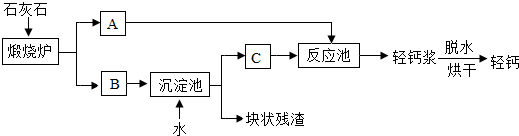
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
 我国建设高铁在促进“一带一路”建设中发挥独特的作用.试回答:
我国建设高铁在促进“一带一路”建设中发挥独特的作用.试回答:查看答案和解析>>
科目:初中化学 来源: 题型:解答题
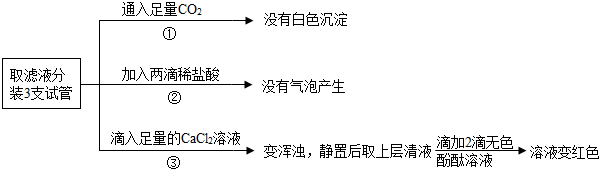
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com