
人类的生产生活离不开金属.
(1)金属铁、铝常用来制作炊具,主要是利用其 性.
(2)人类每年从自然界提取大量的金属,其中提取量最大的是铁.赤铁矿(主要成分为Fe2O3)和一氧化碳炼铁的化学方程式为 .
(3)我国钢铁年产量很高,但因锈蚀造成的损失也很惊人.工业上常用稀盐酸除去铁锈,该反应的化学方程式为 .
(4)从含有CuSO4、ZnSO4、FeSO4的废水中回收重要原料硫酸锌和有关金属,实验过程如下.
请回答:
写出步骤①中发生反应的化学方程式 ;固体D的化学式为 ;以上物质A~G中,含有锌元素的是 (填字母序号)
(1)导热; (2)3CO+Fe2O3 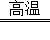 2Fe+3CO2;(3)6HCl+Fe2O3=2FeCl3+3H2O;
2Fe+3CO2;(3)6HCl+Fe2O3=2FeCl3+3H2O;
(4)Zn+FeSO4=Fe+ZnSO4 ;Zn+CuSO4=ZnSO4+Cu;Fe;ABCEG.
解析试题分析:(1)作炊具,主要是利用金属的导热性.(2)用赤铁矿(主要成分为Fe2O3)和一氧化碳炼铁的反应物是一氧化碳和氧化铁,写在等号的左边,生成物铁和二氧化碳写在等号的右边,根据得失氧进行配平,反应条件是高温写在等号的上边,所以化学方程式为:3CO+Fe2O3 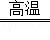 2Fe+3CO2.(3)盐酸除铁锈的反应物是盐酸和氧化铁写在等号的左边,生成物氯化铁和水写在等号的右边,用观察法配平即可,所以方程式是:6HCl+Fe2O3=2FeCl3+3H2O.(4)根过量A是加入的锌,锌与硫酸亚铁反应生成铁和硫酸锌,所以方程式是:Zn+FeSO4═Fe+ZnSO4;锌与硫酸铜反应生成铜和硫酸锌,所以方程式是:Zn+CuSO4═ZnSO4+Cu;由于锌与硫酸亚铁反应生成铁盒硫酸锌,锌与硫酸铜反应生成铜和硫酸锌,且加入的锌是过量的,所以固体B中含有锌、铁、铜;溶液C是硫酸锌溶液;固体B用磁铁把铁吸引出来,所以固体D是铁;固体E中含有锌和铜,由于锌能与硫酸反应,铜与硫酸不反应,所以加入的溶液F是稀硫酸,溶液G是硫酸锌溶液;所以含有锌元素的有ABCEG.
2Fe+3CO2.(3)盐酸除铁锈的反应物是盐酸和氧化铁写在等号的左边,生成物氯化铁和水写在等号的右边,用观察法配平即可,所以方程式是:6HCl+Fe2O3=2FeCl3+3H2O.(4)根过量A是加入的锌,锌与硫酸亚铁反应生成铁和硫酸锌,所以方程式是:Zn+FeSO4═Fe+ZnSO4;锌与硫酸铜反应生成铜和硫酸锌,所以方程式是:Zn+CuSO4═ZnSO4+Cu;由于锌与硫酸亚铁反应生成铁盒硫酸锌,锌与硫酸铜反应生成铜和硫酸锌,且加入的锌是过量的,所以固体B中含有锌、铁、铜;溶液C是硫酸锌溶液;固体B用磁铁把铁吸引出来,所以固体D是铁;固体E中含有锌和铜,由于锌能与硫酸反应,铜与硫酸不反应,所以加入的溶液F是稀硫酸,溶液G是硫酸锌溶液;所以含有锌元素的有ABCEG.
考点:金属的物理性质及用途;金属活动性顺序及其应用;一氧化碳还原氧化铁;酸的化学性质.


 名师指导期末冲刺卷系列答案
名师指导期末冲刺卷系列答案 开心蛙口算题卡系列答案
开心蛙口算题卡系列答案科目:初中化学 来源: 题型:问答题
矿物的储量有限且不能再生。根据已探明的一些矿物储藏量,并根据目前这些金属的消耗速度,有人估计一些矿物的开采年限如下图所示(不包括今后新探明矿物储量,一些国家金属储备量和金属的回收利用等)回答问题:
(1)写出保护金属资源的方法(要求至
少写两种不同的方法)。
① ;
② 。
(2)地壳中元素的含量排在前四位的是 (用元素符号表示)
(3)用下列试剂验证铝、铁、铜三种金属的活动性顺序,能达到目的的是 (填序号)。
A.硫酸铝溶液 B.硫酸亚铁溶液 C.硫酸铜溶液
(4)人们大量使用的是合金而不是纯金属,这是因为合金具有更多优良性能,例如钢比纯铁硬度 (填“大”或“小”)。
查看答案和解析>>
科目:初中化学 来源: 题型:探究题
(7分)冬天,小方陪妈妈去医院打点滴,发现护士往输液管上放了一个纸包(如图所示),经询问得知它可以温暖输入人体中的液体。小方对包里的东西能产生热量感到很神奇,于是,他向护士要了一只用过的纸包,带回来进行了如下探究。
探究一:包里是什么物质。
他剪开纸包,发现里面是一些黑色粉末和暗红色粉末。
【提出猜想】纸包里的物质可能是炭粉、铁粉、氧化铁、氧化亚铁中某几种物质的混合物。
【查阅资料】氧化亚铁是一种黑色粉末,不溶于水。在空气中稍受热即被迅速氧化成四氧化三铁,铁的氧化物中只有四氧化三铁能被磁铁吸引。四氧化三铁与盐酸反应生成氯化亚铁、氯化铁和水。
【初步结论】根据资料知识,你认为纸包中的黑色粉末除了猜想物质以外,还可能含有 。
【进行实验】
| 实验编号 | 实验操作 | 实验现象 |
| ① | 将磁铁靠近粉末 | 黑色粉末部分被吸引,暗红色粉末不被吸引 |
| ② | 取少量粉末加入足量稀盐酸 | 有气泡产生,底部有黑色不溶物 |
| 实验步骤 | 实验现象 | 结论 |
| | | 纸包中含有四氧化三铁。 |
查看答案和解析>>
科目:初中化学 来源: 题型:探究题
下表是某种常见金属的部分性质:
| 颜色、状态 | 硬度 | 密度 | 熔点 | 导电性 | 导热性 | 延展性 |
| 银白色固体 | 较软 | 2.70g/cm3 | 660.4℃ | 良好 | 良好 | 良好 |
| 你的一种猜想 | |
| 验证方法 | |
| 现象 | |
| 结论 | |
查看答案和解析>>
科目:初中化学 来源: 题型:探究题
某化学兴趣小组对金属的性质做了如下探究,请你填写空格:
(1)用如图所示实验探究铁生锈的条件(每支试管中均放有完全相同的洁净铁钉):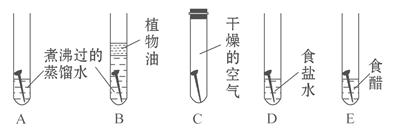
①甲同学认为:试管A发生的现象就能够说明铁的锈蚀是铁与空气中的氧气、水蒸气共同作用的结果。乙同学不同意他的观点,认为必须全面观察试管_________(填试管编号)发生的现象,并经过科学严谨的推理,才能得出上述结论。
②试管D和E实验的目的是进一步探究铁在_______的环境中是否更容易锈蚀。
③为防止金属锈蚀,除了采用覆盖保护膜等措施以外,还可以制成合金。这是因为合金与纯金属相比,其组成和内部结构发生变化,从而引起____________的变化。
(2)某同学向分别盛有等质量的铁粉和锌粒的试管中,倒入等质量、等溶质质量分数的稀硫酸,以“金属表面产生气泡的快慢”为标准来判断两种金属的活动性强弱。有的同学认为这种方案不够合理,理由是_________________________________________________________________________。
(3)将一定质量的铁粉放入硝酸铜、硝酸锌的混合溶液中,充分反应后过滤,所得固体中一定含有的物质是________,且反应后溶液质量比反应前________(填“增大”“减小”或“不变”)。
查看答案和解析>>
科目:初中化学 来源: 题型:计算题
现有 100 t含氧化铁80%的赤铁矿石,工业上用于冶炼生铁
(1)生铁主要是铁和 的合金;
(2)100 t含氧化铁80%的赤铁矿石中氧化铁的质量= t ;
(3)用题中所给的赤铁矿石能冶炼出含杂质3%的生铁多少吨?
高温
(反应的化学方程式为Fe2O3 + 3CO ="2Fe" + 3CO2 )
查看答案和解析>>
科目:初中化学 来源: 题型:信息分析题
A、B、C、D、E、X、Y、Z都是初中化学中的常见物质,其中A是天然气的主要成分,X、Y、Z是单质,B、C、D、E是氧化物,常温下C是液体,Y是黑色固体,E是红棕色粉末。它们之间有如下反应关系:
请根据以上信息回答下列问题:
(1)有关物质的化学式:A为 ,C为 。
(2)B与Y反应的化学方程式为 ,
D与E反应的化学方程式为 。
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
(6分)在实验室里,同学们正在完成粗盐提纯的实验,对于实验得到的精盐样品,能否配制生理盐水,同学们有如下猜想:
【猜想与假设】
甲同学猜想:样品可以用来配制生理盐水;
乙同学猜想:样品不可以用来配制生理盐水;
【表达与交流】
你认为,乙同学猜想的理由是(1) ;
【探究实验一】乙同学取样品溶于水,向溶液中加入氢氧化钡溶液,观察到有白色沉淀生成。过滤后,向滤渣中入足量的稀硝酸,沉淀部分溶解,但无其他现象,再过滤,得到滤液中的溶质和第一次过滤得到的滤液中所含有的阴离子不同。则样品中含有的一种可溶性杂质为(2)___________________________;
丙同学为了验证样品中的杂质,继续向第一次过滤得到的滤液中加入碳酸钠溶液,又观察到有白色沉淀产生,得出结论样品中还含有的另一种可溶性杂质氯化钙。
【反思与评价】请你评价丙同学的结论:(3)___________________________。
【提出问题】如何证明丙同学的结论?
【收集证据】乙同学再取样品溶于水,加入(4)__________溶液,振荡、过滤,向滤液中加入(5)_________溶液观察到(6)___________________________现象证明含有氯化钙。
【表达与交流】请你设计实验方案除去样品中的两种杂质将样品提纯为纯净的氯化钠。取样,依次加入(7)____ ______________三种试剂,过滤,再加入(8)_______________,最后通过蒸发得到可以配制生理盐水的纯净氯化钠固体。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com