
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题

查看答案和解析>>
科目:初中化学 来源: 题型:填空题
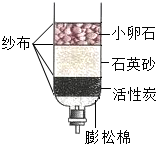 今年四、五月份,我国湖北、江西等地遭遇大范围持续干旱----鄱阳湖干涸等.全国人们团结一致,共同抗旱.
今年四、五月份,我国湖北、江西等地遭遇大范围持续干旱----鄱阳湖干涸等.全国人们团结一致,共同抗旱.查看答案和解析>>
科目:初中化学 来源: 题型:选择题
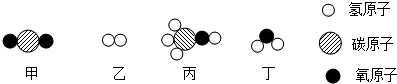
| A. | 丙的相对分子质量为 24 | |
| B. | 生成的丙和丁的分子个数比为 2:1 | |
| C. | 反应前后分子总数不变 | |
| D. | 发生反应的甲和乙的质量比为 22:3 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. |  | B. |  | C. |  | D. |  |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com