
【题目】如图为 A 物质的溶解度曲线,M、N 两点分别表示 A 物质的两种溶液。下列做法不能实现 M、N 间的 相互转化的是(A 从溶液中析出时不带结晶水)( )
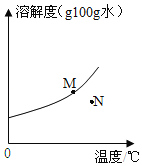
A. 从 M→N:先将 M 降温再过滤,再将其升温
B. 从 M→N:先将 M 升温再将其蒸发掉部分水
C. 从 N→M:先向 N 中加入适量固体 A 再降温
D. 从 N→M:先将 N 降温再加入适量固体 A
 津桥教育计算小状元系列答案
津桥教育计算小状元系列答案科目:初中化学 来源: 题型:
【题目】请结合如图回答问题.
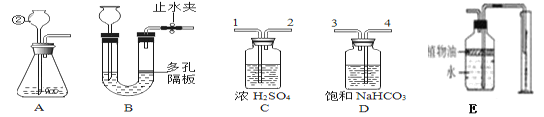
(1)实验室可用A装置制取CO2,其化学方程式为_____,若将A改为B,其优点是___若用装置E收集CO2,并测量生成的CO2气体的体积,其中在水上放一层植物油的目的是___,装置E中植物有上方的空气对测量CO2的体积_____(填“有”或“没有”)影响
(2)为了得到纯净、干燥的CO2,除杂装置导管的正确连接顺序是____(填数字).
(3)若装置C充满水,要想排出装置C中的水,使它充满O2,则氧气应从____(填“1”或“2”)通入。
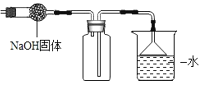
(4)下图是收集某气体的装置,由实验装置推测该气体的有关性质可能是(_____)

查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】请根据下列各图中提供的信息回答问题:
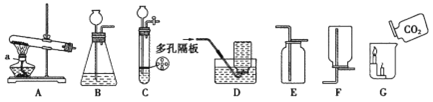
(1)写出仪器a的名称:______。
(2)请写出用装置B制取氧气的化学方程式:______。
(3)比较用过氧化氢溶液和用氯酸钾固体制取O2的方法,两者的共同点是______。
A 发生装置相同
B 都可用MnO2做催化剂
C 完全反应后剩余的固体成分相同
(4)装置B、C都可用来制取二氧化碳,装置C相对于装置B在操作方面的优势是______。
(5)用大理石和稀盐酸制取一瓶二氧化碳气体,将这瓶气体按G所示慢慢倒入烧杯中,观察到蜡烛自下而上依次熄灭,说明二氧化碳具有的性质是______。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】“五一”假期,小兵对“锌与硫酸反应快慢的影响因素”进行了探究。
【提出问题】锌与硫酸反应的快慢受哪些因素的影响呢?
【猜想与假设】a.可能与硫酸的质量分数有关;
b.可能与锌的形状有关。
【设计并实验】小兵用不同质量分数的硫酸和不同形状的锌进行如下实验。
实验 编号 | 硫酸的质量 分数(均取 20 mL) | 锌的形状 (均取1 g) | 氢气的体积(mL) (均收集3分钟) |
① | 20% | 锌粒 | 31.7 |
② | 20% | 锌片 | 50.9 |
③ | 30% | 锌粒 | 61.7 |
④ | 30% | 锌片 | 79.9 |
(1)写出稀硫酸与锌反应的化学方程式:________________________。
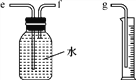
(2)小兵用如图所示装置收集并测量氢气的体积,其中量筒的作用是________________________________________,氢气应从________(填“e”“f”或“g”)管通入。
【收集证据】(3)要比较不同质量分数的硫酸对反应快慢的影响,应选择的实验编号是____________。
【得出结论】(4)结论是________________________________________________________________。
(5)下表是小兵第①组实验的详细数据。
时段(均 为1分钟) | 第1 分钟 | 第2 分钟 | 第3 分钟 | 第4 分钟 | 第5 分钟 | 第6 分钟 |
H2的体积 | 3.1 mL | 16.7 mL | 11.9 mL | 9.6 mL | 7.6 mL | 6.0 mL |
请描述锌与硫酸反应的快慢的变化并解释原因:______________________________。
(6)锌与硫酸反应的快慢可能还受哪些因素影响?设计实验验证。___________________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】下面是甲、乙实验小组完成的相关实验。
甲小组:利用下图装置研究燃烧条件(已知白磷的着火点为40℃)。
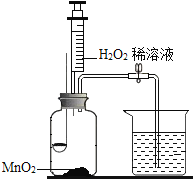
步骤Ⅰ:烧杯中盛有80℃的热水,分别在燃烧匙和烧杯中导管口放置一小块白磷,塞紧瓶塞。
步骤Ⅱ:用注射器向瓶内推入适量H2O2 溶液
(1)H2O2稀溶液与MnO2接触时发生反应的文字表达式为_____;
(2)实验中,推入H2O2溶液前,燃烧匙中的白磷不燃烧,原因是_____;推入H2O2溶液后,观察到烧杯中的现象是_____。
乙小组:哪些因素影响过氧化氢分解的速率?
实验序号 | H2O2溶 液浓度% | H2O2溶液体积/mL | 温度℃ | MnO2的用量/g | 收集氧气的体积/mL | 反应所需 的时间/s |
① | 5 | 1 | 20 | 0.1 | 4 | 16.75 |
② | 15 | 1 | 20 | 0.1 | 4 | 6.04 |
③ | 30 | 5 | 35 | 2 | 49.21 | |
④ | 30 | 5 | 55 | 2 | 10.76 |
(1)通过实验对比可知,化学反应速率与浓度和温度有关系。
(2)化学反应的实质是微观粒子相互接触、碰撞的结果,化学反应速率与微观粒子相互接触、碰撞的概率有关。试从微观角度解释“反应物浓度越大,化学反应速率越快”的原因是:_____;
(3)用一定量15%的过氧化氢溶液制氧气,为了减小反应速率,可加适量的水稀释,产生氧气的总重量_____(填“减小”或“不变”或“增大”)。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】水是生活生产中不可缺少的物质。

①日常生活和生产中常见的水,属于纯净物的是_____。
A 矿泉水 B 蒸馏水 C 河水 D 雨水
②如图甲所示的简易净化水的装置,运用了如下净水方法中的_____(填序号)。
A 消毒 B 过滤 C 蒸馏 D 吸附
③保持水的化学性质的微粒是_____(填名称),图乙中电解水的化学方程式是_____,b 试管中产生的气体是_____,检验该气体的方法是_____,实验说明水是_____由组成的。
④水中滴入几滴石蕊试液,向其中通入二氧化碳气体,可看到石蕊试液变_____色,其反应原理是_____(用化学方程式表示),该原理也可用于制碳酸饮料。打开可乐瓶有大量气泡逸出,说明压强减小,气体溶解度变_____(填“大”或“小”),当气泡逸出后,瓶内的液体_____(填“是”或“不是”)二氧化碳的饱和溶液。
⑤20℃,食盐的溶解度是 36g/100g 水,此时饱和溶液的溶质的质量分数是 26.5%.则“100g”表示_____;“%”表示_____。
A 溶质质量 B 溶剂质量 C 溶液质量 D 溶液体积
⑥将 15g 下列物质投入 85g 水中,使之充分溶解,试比较所得溶液的溶质质量分数的大小_____。
a.二氧化硫 b.氯化钠 c.硫酸铜晶体 d.氧化钙
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】(9分)2011年3月,日本强烈地震后,海啸引发福岛第一核电站的放射性物质外泄,有关131I(碘-131)的相关报道成为热门话题。请回答下列问题:
(1)131I原子中含有53个质子,78个中子。
①131I原子的核外电子数为__________。
②自然界中普遍存在另一种稳定的碘原子127I,它和131I同属于碘元素。127I原子的质子数为__________。
(2)专家指出,服用碘片(有效成分为KI)可以治疗131I造成的辐射,但服用碘酒(有效成分为I2)却会引起碘中毒。KI和I2的性质不同的原因是______ ___。
(3)日本地震后,个别居民抢购食盐。假设某人经医生确认,每日需要补充166 mg KI。已知每千克某品牌碘盐中KIO3的加入量为42.8 mg,如果用该食盐替代碘片提供治疗辐射所需的碘元素,则每日需食用该食盐的质量为__________kg。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】以下是Na2CO3、NaHCO3的溶解度表。下列说法中错误的是( )
0℃ | 10℃ | 20℃ | 30℃ | 40℃ | 50℃ | 60℃ | |
Na2CO3的溶解度(g/100g水) | 7.1 | 12.5 | 21.5 | 39.7 | 49.0 | 48.5 | 46.0 |
NaHCO3的溶解度(g/100g水) | 6.9 | 8.1 | 9.6 | 11.1 | 12.7 | 14.5 | 16.4 |
A. 40℃的饱和Na2CO3溶液升温到60℃,会析出晶体
B. 60℃的NaHCO3溶液蒸干并充分灼烧,可得到NaHCO3晶体
C. 30℃的溶质质量分数为25%的Na2CO3溶液降温到20℃,有晶体析出
D. 20℃的饱和Na2CO3溶液中通足量CO2,生成的NaHCO3会部分析出
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】下图是某学生学习化学知识后进行的归纳,你认为相应图示表示正确的是( )
A. ![]() 氮元素的化合价
氮元素的化合价
B. ![]() 碳元素的质量分数
碳元素的质量分数
C. ![]() 含碳量
含碳量
D. ![]() 金属活动性
金属活动性
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com