
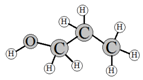
 丙醇在很多情况下可代替沸点较低的乙醇用作有机溶剂,如图是丙醇的分子结构图,其化学式为C3H7OH.下列有关丙醇的说法正确的是( )
丙醇在很多情况下可代替沸点较低的乙醇用作有机溶剂,如图是丙醇的分子结构图,其化学式为C3H7OH.下列有关丙醇的说法正确的是( )| A. | 丙醇是由碳、氢、氧三种原子构成的 | |
| B. | 丙醇中碳、氢、氧的质量比为3:8:1 | |
| C. | 丙醇中氢元素的质量分数最大 | |
| D. | 丙醇不属于氧化物,但属于有机化合物 |
分析 A.根据物质的结构来分析;
B.根据化合物中元素的质量比来分析;
C.根据化合物中元素的质量分数计算方法来分析;
D.根据氧化物与有机物的概念来分析.
解答 解:A.丙醇是由丙醇分子构成的,而不是由原子直接构成的,故错误;
B.丙醇(C3H7OH)中碳、氢、氧的质量比为:(12×3):(1×8):16=36:8:16≠3:8:1,故错误;
C.丙醇(C3H7OH)中碳、氢、氧的质量比为:(12×3):(1×8):16=36:8:16=9:2:4,可见其中碳元素的质量分数最大,故错误;
D.氧化物是由两种元素组成的化合物,丙醇(C3H7OH)中含三种元素,不属于氧化物,该物质是含碳元素的化合物,属于有机化合物,故正确.
故选D.
点评 本题考查了化学式的意义以及化学式的计算方法,难度不大.


科目:初中化学 来源: 题型:选择题
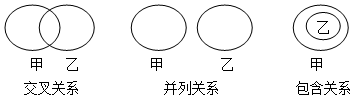
| A. | 碱性溶液和碱溶液:包含关系 | B. | 复分解反应和中和反应:并列关系 | ||
| C. | 氧化物和化合物:交叉关系 | D. | 化学肥料和复合肥料:并列关系 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| 物质 | 所含杂质 | 除去杂质的试剂与操作 | |
| A | FeCl2溶液 | CuCl2 | 过量锌粉,过滤 |
| B | Cu | CuO | O2,加热 |
| C | KCl | KClO3 | MnO2,加热 |
| D | CaCl2溶液 | 稀盐酸 | 过量CaCO3,过滤 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题

查看答案和解析>>
科目:初中化学 来源: 题型:计算题
| 加入氯化钙溶液次数 | 第一次 | 第二次 | 第三次 |
| 生成沉淀的总质量/g | 4 | m | 10 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A | 不同物质性质不同,鉴别方法不同 | 氧化铜与碳粉一一在空气中灼烧 |
| B | 物质在微观上都是由粒子构成的 | 铁一一由分子构成 |
| C | 物质的性质决定了它的反应现象 | 向NaOH溶液中滴加紫色石蕊试液一一溶液变为红色 |
| D | 混合物除去杂质(括号内为杂质) | FeSO4溶液(稀H2SO4)一一加入过量的氧化铁,过滤 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 植树造林,绿化家园 | B. | 推广使用太阳能、风能 | ||
| C. | 骑公共自行车出行 | D. | 露天焚烧秸秆和垃圾 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
| 氢氧化物 | Fe(OH)3 | Al(OH)3 | |
| 开始沉淀时的pH | 2.3 | 4.0 | 开始溶解:7.8 |
| 完全沉淀时的pH | 3.7 | 5.2 | 完全溶解:10.8 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com