
| A. | 放热 | B. | 发出耀眼的白光 | C. | 生成白色固体 | D. | 冒出白烟 |
科目:初中化学 来源: 题型:解答题
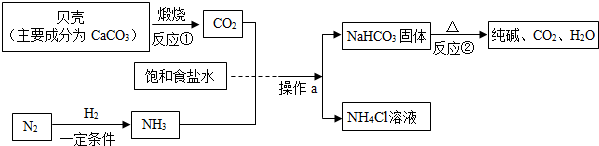
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 扩大公共绿地,打造绿色家园 | B. | 鼓励燃煤发电,保障电力供应 | ||
| C. | 禁止秸杆燃烧,减轻雾霾影响 | D. | 发展公共交通,提倡低碳生活 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
| 实验操作 | 预测现象 | 结论 |
| 取少量反应后的溶液于烧杯中,并向其中滴加足量的 碳酸钠溶液. | 先有气泡产生且溶液中出现沉淀 | 猜想乙正确 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
| 实验操作 | 实验现象 | 实验结论 |
| ①取少量样品放入试管中,加入一定量的盐酸 | 有气泡出现 | 猜想二成立 |
| ②另取少量样品放入试管中,加入适量水,静置后向上层清液中滴加 碳酸钠溶液 | 产生变色沉淀 | |
| ③另取少量样品放入试管中,加入适量水,静置后向上层清液中滴加 酚酞试液 | 酚酞试液不变色 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 它是一种不同于水的物质 | B. | 它是混合物 | ||
| C. | 它的分子之间有间隔 | D. | 它的分子不再运动 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
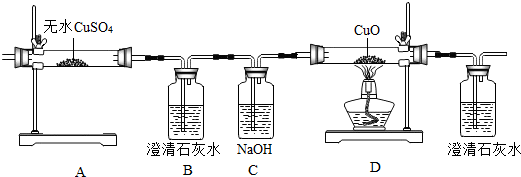
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
| 实验操作 | 预测现象 | 结论 |
| 取少量反应后的溶液于烧杯中,并向其中滴加足量的碳酸钠溶液. | 有气泡产生且溶液中出现沉淀 | 猜想乙正确 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com