
分析 (1)根据酒精灯使用的注意事项分析;
(2)
解答 解:(1)酒精灯不小心被碰倒,洒出的酒精在桌上燃烧起来,应该立即用湿抹布扑灭,这样即可以隔绝空气,又可以降低温度,可以达到灭火的目的.
故填:湿抹布扑灭;(2)在用酒精灯给试管内液体加热时,试管外边有水,容易导致试管受热不均匀使试管炸裂;试管底部接触焰心因为外焰温度最高,焰心温度较低,使试管受热不均匀容易炸裂试管;没有进行预热直接集中加热试管内的液体,这样会使试管受热不均炸裂试管;
故填:试管外边有水;没有进行预热直接集中加热试管内的液体.
点评 本考点属于考查实验基本操作题,特别考查了实验过程中的注意事项,要仔细分析,认真处理.本考点经常出现在填空题和实验题中.


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:初中化学 来源: 题型:实验探究题
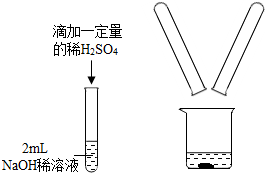 实验课上各小组同学们在实验室做了酸碱反应的实验.
实验课上各小组同学们在实验室做了酸碱反应的实验.| 实验步骤 | 预期的实验现象 | 实验结论 |
| 取少量混合液于试管中,滴入碳酸钠溶液 | 小明的猜想正确 |
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
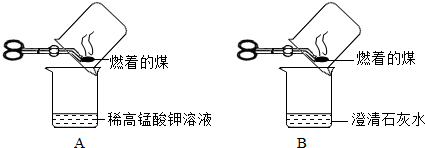
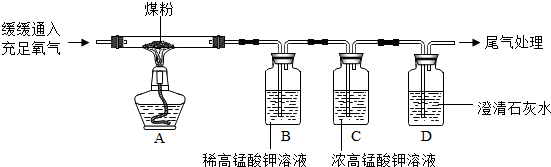
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com