
| 实验操作 | 实现现象 | 实验结论 |
① X是碳酸钠溶液 X是碳酸钠溶液 | 无明显现象 | 猜想二不正确 |
② Y是氢氧化钙溶液 Y是氢氧化钙溶液 | 产生白色沉淀 | 猜想三正确 |
分析 (1)碳酸钠和氢氧化钙反应生成白色沉淀碳酸钙和氢氧化钠;
【交流讨论】二氧化碳能和氢氧化钙反应生成碳酸钠和水,能和氢氧化钙反应生成碳酸钙沉淀和水;
【实验评价】稀盐酸能和氢氧化钠反应生成氯化钠和水,能和碳酸钠反应生成氯化钠、水和二氧化碳.
解答 解:(1)碳酸钠和氢氧化钙反应生成白色沉淀碳酸钙和氢氧化钠,反应的化学方程式为:Na2CO3+Ca(OH)2═CaCO3↓+2NaOH.
故填:Na2CO3+Ca(OH)2═CaCO3↓+2NaOH.
【实验探究】如果向样品溶液中滴加碳酸钠溶液,无明显现象,说明溶液中不含有氢氧化钙;
如果向样品溶液中滴加氢氧化钙溶液,产生白色沉淀,说明溶液中含有碳酸钠,填表如下所示:
| 实验操作 | 实现现象 | 实验结论 |
①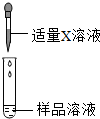 X是碳酸钠溶液 X是碳酸钠溶液 | 无明显现象 | 猜想二不正确 |
② Y是氢氧化钙溶液 Y是氢氧化钙溶液 | 产生白色沉淀 | 猜想三正确 |
点评 往样品溶液中通入二氧化碳气体时,如果溶液中含有氢氧化钙,则二氧化碳和氢氧化钙反应生成白色沉淀碳酸钙,如果二氧化碳先和氢氧化钠反应,则反应生成的碳酸钠能和氢氧化钙反应生成白色沉淀碳酸钙,如果无明显现象,说明溶液中不含有氢氧化钙.


科目:初中化学 来源: 题型:选择题
| A. | CuSO4 NaCl KNO3 | B. | NaOH NaCl NaNO3 | ||
| C. | Na2SO4 NH4Cl ZnCl2 | D. | K2SO4 AgNO3 NaCl |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
 以物质的类别为横坐标,化合价为纵坐标绘制的图象,如图是铁的价类图,Y物质为( )
以物质的类别为横坐标,化合价为纵坐标绘制的图象,如图是铁的价类图,Y物质为( )| A. | FeO | B. | Fe(OH)2 | C. | Fe3O4 | D. | FeSO4 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
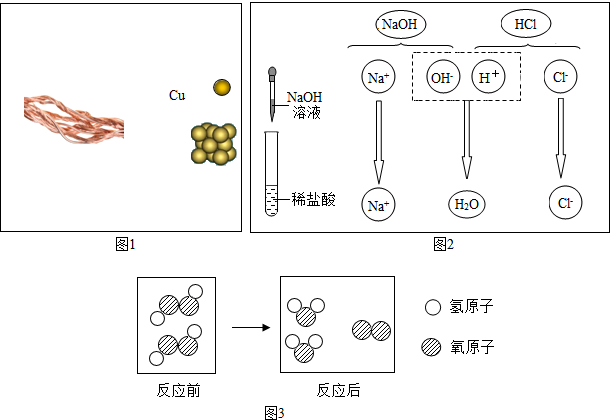
查看答案和解析>>
科目:初中化学 来源: 题型:推断题
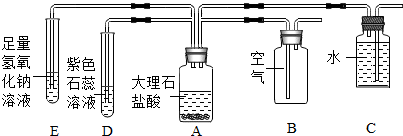
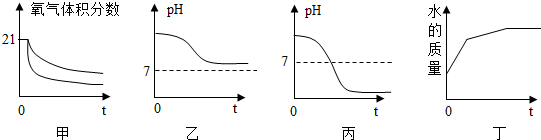
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
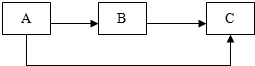 A、B、C为初中化学常见物质,它们之间的转化关系如图所示(反应条件、部分反应物和生成物已略去).
A、B、C为初中化学常见物质,它们之间的转化关系如图所示(反应条件、部分反应物和生成物已略去).查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 若滤液中有Cu2+,则一定含有Fe2+ | |
| B. | 若滤液中无Cu2+,则溶液中一定含有Zn2+和Fe | |
| C. | 若滤渣中有Fe,则滤液中一定没有Cu2+,滤渣中可能含有Zn | |
| D. | 若滤渣中有Zn,则滤液中无Cu2+,不可能含有Fe2+ |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
| 主要成分 | NaHCO3 | Mg(OH)2 |
| 主要成分相对分子质量 | 84 | 58 |
| 建议每次剂量/g | 0.5 | 0.3 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com