
【题目】取22.2g石灰石样品,放入盛有126g稀盐酸的烧杯中,石灰石中的CaCO3与盐酸恰好完全反应(杂质不反应,也不溶解),烧杯内物质质量变为139.4g。请计算:
(1)反应生成 二氧化碳的质量;
(2)反应后所得溶液中溶质的质量分数。(保留一位小数)
【答案】
(1)
m(CO2)= 126g+22.2g-139.4g=8.8g
(2)
解:反应后溶液的溶质为CaCl2,
则设CaCO3的质量为x,的质量为y,CaCl2
CaCO3+ | 2HCl= | CaCl2+ | H2O+ | CO2↑ |
100 | 111 | 44 | ||
x | y | 8.8g |
![]()
![]()
解得x=20g
y=22.2g
则CaCl2的质量分数为 ![]() ×100%=16.18%
×100%=16.18%
答:反应后所得溶液中溶质的质量分数为16.18%。
【解析】(1)反应前后减少的质量即为生成气体的质量,则m(CO2)= 126g+22.2g-139.4g=8.8g;(2)反应后的溶质为CaCl2 , 首先需求出CaCl2的质量;因为反应后的烧杯中含有杂质,所以需要知道真正参加反应的CaCO3的质量,方便后面求出溶液的总质量;则设CaCO3的质量为x,的质量为y,CaCl2
CaCO3+ | 2HCl= | CaCl2+ | H2O+ | CO2↑ |
100 | 111 | 44 | ||
x | y | 8.8g |
![]()
![]()
解得x=20g
y=22.2g
则CaCl2的质量分数为 ![]() ×100%=16.18%
×100%=16.18%
【考点精析】掌握质量守恒定律及其应用和根据化学反应方程式的计算是解答本题的根本,需要知道①质量守恒定律只适用于化学变化,不适用于物理变化;②不参加反应的物质质量及不是生成物的物质质量不能计入“总和”中;③要考虑空气中的物质是否参加反应或物质(如气体)有无遗漏;各物质间质量比=系数×相对分子质量之比.


科目:初中化学 来源: 题型:
【题目】食用碱的主要成分是Na2CO3(常含有少量的NaCl),课外探究小组为测定市售食用碱中Na2CO3的含量,设计了如图实验装置. 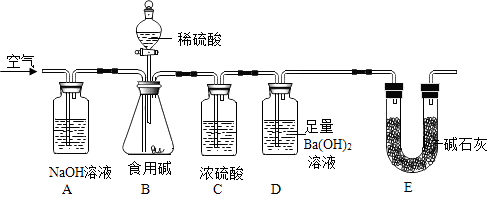
设计思路:用空气将装置B中生成的二氧化碳缓缓吹入装置D中,利用装置D的质量变化测定食用碱中Na2CO3的含量,请结合实验装置和设计思路,回答下面问题:
(1)装置D中发生反应的化学方程式为;
(2)装置E的作用是;
(3)缓缓通入空气的目的是;
(4)若撤出装置A,直接通入空气会导致实验结果(填“偏大”、“偏小”或“不变”,下同),若撤除装置C,对实验结果的影响是 .
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】A~M均为初中化学常见物质,其中A是大理石主要成分,B是人体胃酸的一种主要成分,F是澄清石灰水主要成分,E是钠盐,它们之间有如图所示的相互转换关系 (图中部分生成物已略去)。请回答下列问题:
(1)E的化学式为 , 请画出K所含元素的原子结构示意图 。
(2)电解J时,通常加入少量烧碱或硫酸的目的是。电解一段时间后在相同条件下,生成气体L和气体K的体积之比约为
(3)I在K中燃烧反应⑥的基本反应类型为。
(4)写出化学方程式:
②
⑤
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】如图是“尾气催化转换器”将汽车尾气中有毒气体转变为无毒气体的微观示意图,其中不同的圆球代表不同原子.下列说法错误的是( ) 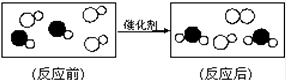
A.化学反应前后元素的种类不变
B.化学反应前后原子数目不变
C.参加反应的两种分子的个数比为3:2或2:3
D.原子是化学变化中的最小粒子
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】实验室常用加热氯酸钾与二氧化锰的混合物的方法制取氧气。
(1)写出反应的文字表达式: .
(2)某化学兴趣小组发现:氯酸钾与氧化铜混合加热,也能较快产生氧气,于是进行如下探究:
【提出猜想】:除二氧化锰、氧化铜外,氧化铁也可以作氯酸钾分解的催化剂.
【完成实验】按下表进行实验,并测定分解温度(分解温度越低,催化效果越好).
实验编号 | 实验用品 | 分解温度 |
1 | 3.0g氯酸钾 | 580 |
2 | 3.0g氯酸钾和1.0g二氧化锰 | 350 |
3 | 3.0g氯酸钾和1.0g氧化铜 | 370 |
4 | x g氯酸钾和1.0g氧化铁 | 390 |
【分析数据,得出结论】
①实验4中x的值应为 , 由实验与实验4对比,证明猜想合理
②实验所用的三种物质中,催化效果最好的是 .
③【反思】若要证明氧化铁是该反应的催化剂,还要验证它在化学反应前后的质量和不变.
(3)【继续探究】小组同学完成上述实验后,又深一步进行“氧化铜用量与一定质量氯酸钾制取氧气反应速率关系”的探究,下表是他们的有关实验数据,请你回答有关问题:
氧化铜与氯酸钾的质量比 | 1/40 | 1/20 | 1/10 | 1/5 | 1/3 | 1/2 | 2/3 | 1/1 | 2/1 |
生成1L氧气所需的时间(s) | 124 | 79 | 50 | 54 | 75 | 93 | 106 | 153 | 240 |
【分析整理】
①据上表可知氧化铜用量过多,产生氧气的速率(填“变快”、“变慢”或“不变”),氧化铜与氯酸钾的质量比为时,反应速率最快.
②【结论1】在化学反应中催化剂的用量(填“是”或“不是”)越多越好.
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】洪涝地区的灾民用下列几个步骤将河水转化为可饮用水.①化学沉降(用明矾),②消毒杀菌(用漂白粉),③自然沉降,④加热煮沸.以上处理过程顺序合理的是( )
A.③②①④ B.③①②④ C.③①④② D.①③④②
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com