
分析 (1)根据溶液稀释前后溶质物质的量不变计算所需浓硫酸的体积;根据所需浓硫酸体积选择量筒规格.
(2)分析操作对溶质的物质的量或对溶液的体积的影响,根据c=$\frac{n}{v}$分析判断.
解答 解:(1)浓配制100mL3.0mol/L的稀H2SO4,需选择100mL容量瓶,根据稀释定律,稀释前后溶质的物质的量不变,来计算浓硫酸的体积,设浓硫酸的体积为xmL,则xmL×18mol/L=100mL×3.0mol/L,解得:x≈16.7mL,所以应量取的浓硫酸体积是16.7mL.量取浓硫酸所用的量筒的规格是25mL.
故答案为:18.4mol/L; B.
(2)A、浓硫酸具有吸水性,浓硫酸长时间放置在密封不好的容器中,浓度会减小,量取的浓硫酸含有的溶质硫酸的物质的量减小,所配溶液浓度偏小;
B、最后需要定容,容量瓶不干燥,含有少量蒸馏水,对溶液浓度无影响;
C、烧杯和玻璃棒未洗涤,会造成溶质的损失,则浓度偏低;
D、定容时俯视刻度线,溶液体积偏小,所配溶液浓度偏大.
故答案:(1)16.7ml;B;(2)A.偏小;B.无影响;C.偏小;D.偏大.
点评 本题考查了一定物质的量浓度溶液的配制,注意从c=$\frac{n}{v}$理解配制原理,注意浓硫酸的稀释操作


科目:初中化学 来源: 题型:选择题
| A. | 一定含有碳、氢两种元素,可能含有氧元素 | |
| B. | 一定含有碳、氢、氧三种元素 | |
| C. | 一定含有碳、氧两种元素,可能含有氢元素 | |
| D. | 只含有碳、氢两种元素,不含有氧元素 |
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 化合反应一定是氧化还原反应 | B. | 分解反应可能是氧化还原反应 | ||
| C. | 置换反应一定是氧化还原反应 | D. | 复分解反应一定不是氧化还原反应 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | NaOH+HCl═NaCl+H2O | |
| B. | Zn+2HCl═ZnCl2+H2↑ | |
| C. | MnO2+4HCl(浓)$\frac{\underline{\;\;△\;\;}}{\;}$MnCl2+2H2O+Cl2↑ | |
| D. | CuO+2HCl═CuCl2+H2O |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
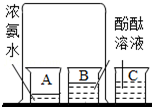 第二章课本中有一个“活动与探究”实验,其实验步骤是:将酚酞溶液分别倒入B、C两个小烧杯中,另取一个小烧杯A,加入约5mL浓氨水.用一个大烧杯罩住A、B两个小烧杯(如图所示)
第二章课本中有一个“活动与探究”实验,其实验步骤是:将酚酞溶液分别倒入B、C两个小烧杯中,另取一个小烧杯A,加入约5mL浓氨水.用一个大烧杯罩住A、B两个小烧杯(如图所示)| 烧杯B | 烧杯C | |
| 现象 | ||
| 解释 | (此处不必填写) |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com