
| 1 |
| 0.02mol |
| 1 |
| x |
| 0.8g |
| 20g |


科目:初中化学 来源: 题型:阅读理解
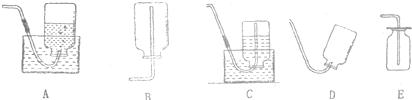
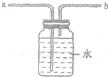

查看答案和解析>>
科目:初中化学 来源: 题型:阅读理解
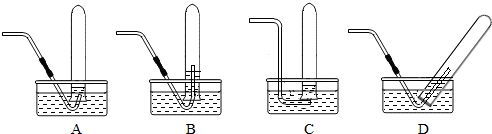
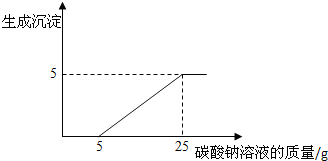
查看答案和解析>>
科目:初中化学 来源: 题型:
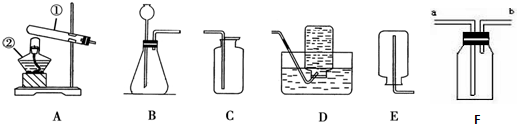
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
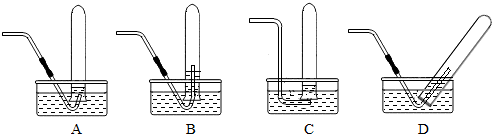

查看答案和解析>>
科目:初中化学 来源:2008-2009学年山东省聊城市临清市九年级(上)期中化学试卷(解析版) 题型:解答题

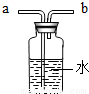
| 实验次序 | 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 |
| H2O2溶液的质量分数 | 1% | 3% | 5% | 10% | 1% | 20% | 25% | 30% |
| MnO2粉末用量/g | 0.2 | 0.2 | 0.2 | 0.2 | 0.2 | 0.2 | 0.2 | 0.2 |
| 收集到540mL气体时所用时间/s | 660 | 220 | 205 | 80 | 25 | 9 | 4 | 3 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com