
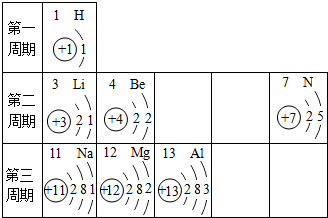
分析 (1)根据氢离子的形成来分析;
(2)根据同一周期元素原子核外电子排布的规律可从周期数与电子层数的关系、最外层电子数的变化进行分析解答.
(3)确定元素种类,然后根据化学式的写法来分析.
解答 解:(1)氢原子的核外只有一个电子,失去后形成氢离子;故填:0;
(2)在元素周期表中,处于同一周期的元素的原子,核外电子层数相同;同一周期元素的原子,从左至右最外层电子数依次增大(合理即可).
故答案为:同一周期的元素的原子,核外电子层数相同;同一周期元素的原子,从左至右最外层电子数依次增大等.
(3)7号是氮元素,常显-3价,12号是镁元素,常显+2价,二者组成的化合物是氮化镁,其化学式为Mg3N2;故答案为:Mg3N2.
点评 本题难度不大,考查学生灵活运用元素周期表的信息、变化规律等进行分析、解题的能力.


 阅读快车系列答案
阅读快车系列答案科目:初中化学 来源: 题型:实验探究题
| 熔点 | 沸点 | 热稳定性 | 其他 |
| 101℃~102℃ | 150℃~160℃升华 | 100.1℃分解出水,175℃分解成CO2、CO、H2O | 与 Ca(OH)2反应产生白色沉淀(CaC2O4) |

查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
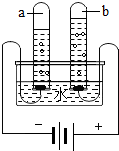 小华和小慧两位同学分别用如图所示的装置进行电解水实验.该反应的化学方程式为2H2O$\frac{\underline{\;通电\;}}{\;}$2H2↑+O2↑.为了增强水的导电性,实验前小华向水中加入硫酸钠固体.则b试管中产生的气体是O2(填化学式),检验这种气体的方法是带火星的木条.
小华和小慧两位同学分别用如图所示的装置进行电解水实验.该反应的化学方程式为2H2O$\frac{\underline{\;通电\;}}{\;}$2H2↑+O2↑.为了增强水的导电性,实验前小华向水中加入硫酸钠固体.则b试管中产生的气体是O2(填化学式),检验这种气体的方法是带火星的木条.| 实验操作 | 实验现象 | 实验结论 |
| ①取少量剩余溶液,滴入氯化铜溶液. | 产生蓝色絮状沉淀 | 溶液中含有氢氧化钠 |
| ②将①中反应后混合物过滤,向滤液中加入足量稀硝酸再滴入几滴硝酸银溶液 | 产生白色沉淀 | 溶液中含有氯化钠 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
| 小倩同学的解法 | 小明同学的解法 |
| 解:设生成的铝质量为X 2Al2O3$\frac{\underline{\;通电\;}}{\;}$4Al+3O2↑ 204108 10t X $\frac{204}{108}$=$\frac{10t}{X}$ X=5.3t 答:最多可生产5.3t铝 | 解:氧化铝中铝元素的质量分数为 $\frac{Al的相对原子质量}{A{l}_{2}{O}_{2}的相对分子质量}$×100% $\frac{27×2}{27×2+16×3}$×100%=53% 铝的质量为10t×53%=5.3t 答:最多可生产5.3t铝 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
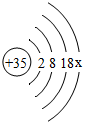 ,该元素符号为Br.图中x=7,Br属于非金属元素(填金属或非金属).下图表示的微粒中,具有相对稳定结构的是C(填序号,下同),与Br化学性质相似的是E.
,该元素符号为Br.图中x=7,Br属于非金属元素(填金属或非金属).下图表示的微粒中,具有相对稳定结构的是C(填序号,下同),与Br化学性质相似的是E.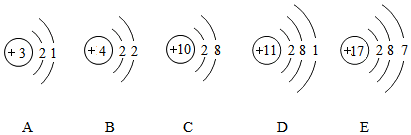
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com