
分析 (1)①根据在化合物中正负化合价代数和为零,结合高铁酸钠的化学式进行解答即可.
②由质量守恒定律:反应前后,原子种类、数目均不变,据此由反应的化学方程式推断生成物X的化学式.
(2)过氧化钠与车厢里的二氧化碳转化为碳酸钠和氧气,写出反应的化学方程式即可.
解答 解:(1)①钠元素显+1价,氧元素显-2价,设铁元素的化合价是x,根据在化合物中正负化合价代数和为零,可得:(+1)×2+x+(-2)×4=0,则x=+6价.
②由质量守恒定律:反应前后,原子种类、数目均不变,由反应的化学方程式Fe2O3+3NaNO3+4NaOH═2Na2FeO4+3NaNO2+2X,反应前铁、氧、钠、氮、氢原子个数分别为2、16、7、3、4,反应后的生成物中铁、氧、钠、氮、氢原子个数分别为2、14、7、3、0,根据反应前后原子种类、数目不变,则2X分子中含有2个氧原子和4个氢原子,则每个X分子由1个氧原子和2个氢原子构成,则物质X的化学式为H2O.
(2)过氧化钠与车厢里的二氧化碳转化为碳酸钠和氧气,反应的化学方程式为2Na2O2+2CO2=2Na2CO3+O2.
故答案为:(1)①+6;②H2O;(2)2Na2O2+2CO2=2Na2CO3+O2.
点评 本题难度不大,掌握利用化合价的原则计算指定元素的化合价的方法、化学反应前后原子守恒来确定物质的化学式、化学方程式的书写方法即可正确解答此类题.


科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 使用节能灯泡 | |
| B. | 近距离出行用自行车代替机动车 | |
| C. | 大力兴建火力发电站以解决人们对电力的需求 | |
| D. | 更多地利用太阳能等能源 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | ①②③④⑤⑥ | B. | ①②③ | C. | ③④⑤ | D. | ④⑤⑥ |
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
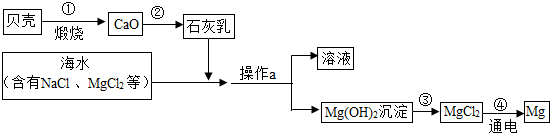
查看答案和解析>>
科目:初中化学 来源: 题型:推断题

查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
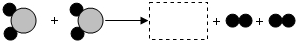
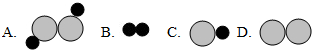
| 物质 | M | N | P | Q |
| 反应前的质量/g | 80 | 1 | 1 | 1 |
| 反应后的质量/g | 1 | 待测 | 45 | 19 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com