
| 盐酸 体积:500mL 化学式:HCl 相对分子质量:36.5 密度:1.2g/cm3 质量分数:37%(1)用该浓盐酸100ml能配制质量分数为20%的盐酸 (2)利用刚配制的稀盐酸来测定某碳酸钠样品的纯度(样品不含氢元素):取50g该样品,向其中滴入刚配好的稀盐酸至不再产生气泡为止,共用去盐酸146g. ①发生反应的化学方程式 ②利用已知条件求解参加反应的固体物质质量(x)的比例式 ③该样品的成分是 ④该样品的纯度是 ⑤若向反应后溶液中加入46.8g水后,此时所得溶液中溶质的质量分数为 分析:(1)利用标签中的说明数据,根据稀释前后溶质质量不变,计算稀释后溶液质量; (2)运用题目意图写出反应的化学方程式;根据化学方程式,利用146g20%的稀盐酸,列出计算碳酸钠质量的比例式;利用碳酸钠质量除以样品质量求出样品纯度; 解答:解:(1)用100mL盐酸可以配制溶质质量分数为20%的盐酸溶液的质量=100mL×1.2g/cm3×37%÷20%=222g 故答案为:222g (2)146g20%的盐酸溶液中HCl质量=146g×20%=29.2设样品中碳酸钠质量为x,反应后生成氯化钠的质量为y,生成二氧化碳的质量为Z. Na2CO3+2HCl=2NaCl+H2O+CO2↑ 106 73 117 44 x 29.2g y z
解得:x=42.4g y=46.8g z=17.6g 则样品中碳酸钠的纯度=
反应后所得溶液的溶质的质量分数为=
答:样品中碳酸钠的质量分数为84.8%. 点评:根据稀释前后溶质质量不变,计算稀释后溶液质量;求出146g20%的盐酸溶液中HCl质量为已知量带入化学方程式求出样品中碳酸钠的质量,这是进一步解决问题的关键.  
练习册系列答案
 阅读快车系列答案 阅读快车系列答案
相关习题
科目:初中化学 来源: 题型: 现有一瓶标签如图所示的浓盐酸,请根据标签上的数据回答问题:
(2)利用刚配制的稀盐酸来测定某碳酸盐样品的纯度(不含氢元素):取一定量该碳酸盐(R2C03)样品,向其中滴入刚配好的稀盐酸至不再产生气泡为止,共用去盐酸73g(杂质不与盐酸反应也不溶于水),然后过滤,得滤渣2.8g,将所得滤液蒸干,得到固体纯净物23.4g. ①发生反应的化学方程式. ③利用已知条件求解参加反应的固体物质质量(x)的比例式 ④该样品的纯度是 ⑤若向反应后溶液中加入31.6g水后,此时所得溶液中溶质的质量分数为 查看答案和解析>> 科目:初中化学 来源: 题型:  现有一瓶标签如图所示的浓盐酸,请根据标签上的数据回答问题: 现有一瓶标签如图所示的浓盐酸,请根据标签上的数据回答问题:(1)要配制165g.20%的盐酸,需用该浓盐酸 (2)利用刚配制的稀盐酸来测定某碳酸盐样品的纯度(不含氢元素):取一定量该碳酸盐(R2C03)样品,向其中滴入刚配好的稀盐酸至不再产生气泡为止,共用去盐酸73g(杂质不与盐酸 反应也不溶于水),然后过滤,得滤渣2.8g,将所得滤液蒸干,得到固体纯净物23.4g. ①发生反应的化学方程式 ②该样品的主要成分化学式的是 ③利用已知条件求解参加反应的固体物质质量(x)的比例式 ④该样品的纯度是 ⑤若向反应后溶液中加入31.6g水后,此时所得溶液中溶质的质量分数为 查看答案和解析>> 科目:初中化学 来源: 题型: 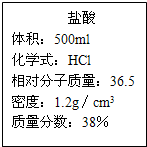 现有一瓶标签如图所示的浓盐酸,请根据标签完成下列问题: 现有一瓶标签如图所示的浓盐酸,请根据标签完成下列问题:(1)用该盐酸50mL能配制质量分数为20%的盐酸 (2)利用刚配制好的盐酸来测定某纯碱样品的纯度:取25g该纯碱样品,向其中滴入刚配制好的盐酸至不再产生气泡为止(样品中杂质不与盐酸反应),共用去盐酸73g,然后将溶液蒸干,得到固体27.2g.求该样品的纯度. 查看答案和解析>> 科目:初中化学 来源: 题型:  (1)氮肥硝酸铵化学式为NH4NO3.其中N元素的化合价为 (1)氮肥硝酸铵化学式为NH4NO3.其中N元素的化合价为-3、+5 -3、+5 ,其氮元素、氢元素、氧元素质量比为7:1:12 7:1:12 .(2)现有一瓶标签如图所示的浓盐酸,请根据标签上的数据回答问题: ①要配制165g20%的盐酸,需用该浓盐酸 100 100 mL.②为从定量角度认识中和反应,小明同学自行设计并进行了下面实验: (Ⅰ)在小烧杯中倒入8%的氢氧化钠溶液l0g,滴入2滴酚酞试剂后,溶液呈红色; (Ⅱ)另取10%的稀盐酸逐滴滴加到氢氧化钠溶液中,边滴边振荡,随盐酸滴入,溶液颜色逐渐变浅; (Ⅲ)在溶液红色消失瞬间,停止实验. 若停止实验时,两溶液恰好反应.请分析小明实验后回答: A、实验中酚酞试剂的作用是 判断中和反应进行的程度 判断中和反应进行的程度 ;B、计算出这时共用去稀盐酸的质量是多少?(精确到0.1) 查看答案和解析>> 同步练习册答案 湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区 违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com版权声明:本站所有文章,图片来源于网络,著作权及版权归原作者所有,转载无意侵犯版权,如有侵权,请作者速来函告知,我们将尽快处理,联系qq:3310059649。 ICP备案序号: 沪ICP备07509807号-10 鄂公网安备42018502000812号 |