
【题目】水的硬度会随着温度的改变而改变。重庆一中某化学兴趣小组利用现有的化学知识,用下图所示装置帮助化学实验室制取少量软水。
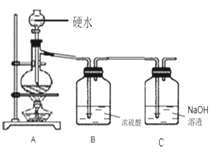
取实验室只含Ca(HCO3)2的硬水500.00ml(密度为a g/mL)进行实验(实验温度不超过100℃),A中发生的化学反应方程式:Ca(HCO3)2![]() CaCO3↓+H2O+CO2↑
CaCO3↓+H2O+CO2↑
实验前测得C的质量为100.00g,反应完全后测得C的质量为100.44g。
(1)浓硫酸的作用是_________________。
(2)生成CO2 质量为_________________g。
(3)实验结束后烧瓶内有多少水垢(沉淀)生成____________(写出计算过程)?
(4)理论上可制得_________g软水。原水的硬度为_________度(提示:每一度即相当于每升水中含10.00mgCaO)。
【答案】 吸收水蒸气 0.44g 1g 500a-1.26 112
【解析】(1)根据浓硫酸具有吸水性分析;(2)根据装置中氢氧化钠的增重可以知道二氧化碳的质量;(3)根据二氧化碳的质量结合方程式计算碳酸钙的质量;(4)根据硬水的质量与沉淀及气体的质量差可以计算软水的质量,结合提示将钙元素的质量转化为氧化钙的质量计算硬度。(1)浓硫酸具有吸水性,因此浓硫酸的作用是吸水干燥二氧化碳的作用;(2)C装置中的氢氧化钠能够吸收二氧化碳,因此反应前后的质量差就是二氧化碳的质量,因此二氧化碳的质量为:100.44g-100g=0.44g;
(3)设产生0.44g二氧化碳的同时得到碳酸钙的质量为x,生成水的质量为y。
Ca(HCO3)2![]() CaCO3↓+H2O+CO2↑
CaCO3↓+H2O+CO2↑
1001844
xy 0.44g
![]()
x=1.00g
y=0.18g
答:生成碳酸钙1.00g。
(4)硬水的质量为500.00ml×ag/mL=500ag,根据反应的方程式可知产生了1.00g的碳酸钙、0.44g二氧化碳,同时会生成0.18g的水,因此得到软水的质量为:500ag-1.00g-0.44g+0.18g=500a-1.26;水的硬度与钙有关,因此1.00g碳酸钙中钙元素的质量为:1.00g×![]() ×100%=0.4g,根据元素的质量不变,可知500ml硬水中氧化钙的质量为:
×100%=0.4g,根据元素的质量不变,可知500ml硬水中氧化钙的质量为: 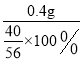 ×1000=560mg,则1L硬水中含有氧化钙的质量为1120mg,因此原水的硬度为112度。
×1000=560mg,则1L硬水中含有氧化钙的质量为1120mg,因此原水的硬度为112度。


科目:初中化学 来源: 题型:
【题目】下列不能用质量守恒定律解释的现象是( )
A.蜡烛燃烧后质量减少B.铁丝生锈后质量增加
C.潮湿的衣服在阳光下晒干D.高锰酸钾加热后固体质量减少
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】下列有关实验现象的描述正确的是( )
A.浓盐酸打开瓶盖后冒出白烟
B.浓氨水中滴加石蕊溶液,溶液变红
C.氯化钠饱和溶液放入少量硝酸钾固体,固体继续溶解
D.铁丝在稀盐酸中反应,溶液逐渐变为黄色
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com