
【题目】现有铜和氧化铜的固体混合物粉末,为研究其组成情况,进行如下实验,请回答下列问题:
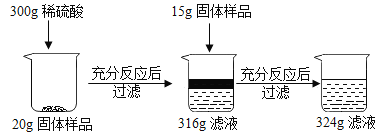
(1)上述实验过程中发生反应的化学方程式为______。
(2)样品中单质Cu的质量分数是______;
(3)第一次反应后所得316g滤液中的溶质是______
(4)根据已知条件列出求解300g稀硫酸中溶质质量(X)的比例式______。
(5)若向最终滤液中加入76g水,所得不饱和溶液中溶质的质量分数为_____
(6)配制上述所需的稀硫酸,需要质量分数为98%的浓硫酸和水的质量比是______。
【答案】CuO+H2SO4=CuSO4+H2O 20% CuSO4、H2SO4 80/98=24g/X 12% 1:9
【解析】
根据300g稀硫酸加入20g固体导致溶液质量增加了16g,说明此时反应的氧化铜的质量为16g。而继续加入15g固体样品,导致溶液质量增加了8g,说明此时稀硫酸完全反应,氧化铜过量。据此结合氧化铜的质量和对应的化学方程式求算稀硫酸中溶质的只以及生成的硫酸铜的质量,进而求算对应的质量分数。
(1)由题意可知,氧化铜能与稀硫酸反应生成了硫酸铜和水,反应的化学方程式是:CuO+H2SO4=CuSO4+H2O;
(2)根据300g稀硫酸加入20g固体导致溶液质量增加了16g,说明此时反应的氧化铜的质量为16g;而继续加入15g固体样品,导致溶液质量增加了8g,反应的氧化铜的总质量为16g+8g=24g,说明此时稀硫酸完全反应,氧化铜过量;样品中铜的质量分数是![]()
![]() 100%=20%;
100%=20%;
(3)根据上面的分析可知,第一次反应后所得316g滤液中的溶质是:剩余的H2SO4和生成的CuSO4;
(4)设稀硫酸中溶质质量为x,生成硫酸铜的质量为y,
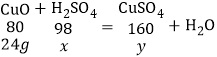
![]() x=29.4g,
x=29.4g,
![]() y=48g,
y=48g,
(5)向最终滤液中加入76g水,所得不饱和溶液中溶质的质量分数为:![]() ×100%=12%;
×100%=12%;
(6)稀硫酸的溶质质量分数是:![]() ×100%=9.8%;设配制上述所需的稀硫酸需要质量分数为98%的浓硫酸和水的质量分别为m、n,则:
×100%=9.8%;设配制上述所需的稀硫酸需要质量分数为98%的浓硫酸和水的质量分别为m、n,则:![]() ×100%=9.8%,
×100%=9.8%,![]() =
=![]() 。
。


科目:初中化学 来源: 题型:
【题目】如图所示是某化学反应的微观示意图,下列说法正确的是_____
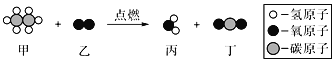
A.该反应属于氧化反应
B.生成物丙由2个氢原子和1个氧原子构成
C.生成物丁中碳、氧元素的质量比为1:2
D.参加反应的甲和乙的分子个数比为_____
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】甲、乙两种固体物质的溶解度曲线如图所示。下列说法正确的是( )
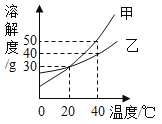
A. 甲的溶解度大于乙的溶解度
B. 将40℃甲的饱和溶液降温至20℃,溶液质量不变
C. 40℃时,分别在100g水中各加入30g甲、乙,同时降温至20℃,甲、乙溶液均为饱和溶液
D. 20℃时,甲溶液中溶质的质量分数一定等于乙溶液中溶质的质量分数
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】下列是实验室制取气体的常用装置,请回答相关问题:
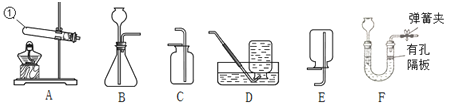
(1)写出仪器①的名称:_____。
(2)实验室用高锰酸钾制备并收集较纯净氧气应选用的装置是_____(填序号)。若用D装置收集氧气时,待集气瓶里的水排完后,接着_____,然后小心地把集气瓶移出水槽,正放在桌面上。
(3)装置B作为气体发生装置对反应物状态和反应条件的要求是_____;用装置C来收集CO2,其验满的方法是_____。 若用装置F制备CO2,其优点是_____。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】国庆佳节家人团聚,丰盛的家宴自然少不了鱼。炖鱼后锅内会残留较多的油渍,可以加入洗涤剂清洗,是利用洗涤剂具有__作用,家用铁锅多为生铁,用完后擦洗不净常会生锈,铁锈主要成分的化学式为__;在铁锅表面加膜不仅起到不粘锅,而且还能防止锅内表面生锈,其防锈原理是___;

家宴自然也少不了同学们爱喝的可乐,当打开可乐时常会有液体溢出的现象,是因为可乐中溶有二氧化碳气体,打开瓶盖后__减小,__减小,气体逸出将可乐带出。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】青少年处在生长发育期,应注意营养均衡,膳食合理。
(1)有些青少年不爱吃蔬菜、水果,影响生长发育,这主要是由于摄入_____(填序号)不足而引起的。
①维生素 ②油脂 ③蛋白质
(2)“××糕点”主要营养成分如图所示。请根据该表回答。
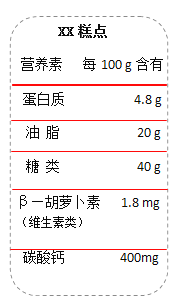
①所含营养素中属于无机盐的是_____(写化学式)。
②其中提供能量的营养素有蛋白质、_____、糖类。
③食用300g该糕点,为人体提供钙元素的质量是_____mg。
(3)直接参与人体新陈代谢活动的糖类是_____(用化学式表示),写出该物质在大自然中产生过程的名称_____。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】研究性学习小组测定实验室里一瓶久置的NaOH固体是否变质.
【提出问题】NaOH固体是否变质?
【猜想与假设】猜想1:没变质,全部是NaOH;
猜想2:全变质,全部是Na2CO3
猜想3:部分变质,既含有NaOH,又含有Na2CO3;
【设计方案并进行实验】请你与他们一起完成,并回答所给问题.
实验步骤 | 实验现象 | 实验结论 |
①称取上述固体样品8g溶于100mL水配成溶液,向溶液中滴加 过量的氯化钙溶液充分反应后,静置. | _________ | 说明久置固体中,一定含有Na2CO3 |
②用玻璃棒蘸取少量①中的上层清液滴在pH试纸上,与标准比色卡对比,测出pH | pH=10 | 说明固体中,还一定含有 _________ (填化学式). |
上述步骤①中,滴加过量氯化钙溶液的目的是 _________
【实验结论】通过实验,说明上述猜想中 _________ 是正确的.
【拓展】
(1)为测定出该NaOH固体的变质程度,继续将上述白色沉淀过滤、洗净、干燥,称得其质量为2g,则固体样品中NaOH的质量分数为 _________ (假定试剂中无其它杂质).
(2)要除去氢氧化钠中含有的碳酸钠,所用的方法(用化学方程式表示) _________
【反思】通过探究,实验室中的氢氧化钠应密封保存.
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】如图是硫粉和铁丝在氧气中燃烧的实验。
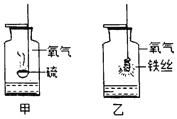
(1)硫在氧气中燃烧比空气中更旺,火焰呈_____色,说明燃烧的剧烈程度与_____有关。
(2)铁丝上系一根火柴的作用是_____,铁丝绕成螺旋状的作用是_____
(3)实验甲中水的作用是_____,实验乙中水的作用是_____
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】用化学符号填空。
(1)3个氢分子_______ (2)镁元素_______
(3)硝酸根离子_______ (4)氢氧化铝中铝元素的化合价_______
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com